Autofagia: cos'è, definizione, meccanismi e importanza biologica
Autofagia: definizione e meccanismi spiegati, ruolo nel riciclo cellulare e nella sopravvivenza, scoperte chiave e implicazioni per salute e ricerca.
Autofagia (dal greco, "mangiare se stesso") è un processo cellulare fondamentale che consente la degradazione e il riciclo di componenti intracellulari danneggiati, superflui o potenzialmente pericolosi. Grazie all'autofagia la cellula mantiene l'omeostasi, si adatta a condizioni di stress (per esempio la fame) e rimuove aggregati proteici o organelli difettosi, trasformando i loro componenti in substrati riutilizzabili per la sintesi e la produzione di energia.
Tipi principali di autofagia
Si riconoscono tre forme principali:
- Macroautofagia: la più studiata. Parti del citoplasma (organelle, aggregati proteici) vengono isolate in una vescicola a doppia membrana chiamata autofagosoma (vescicola a doppia membrana). L'autofagosoma si fonde poi con i lisosomi, dove il contenuto viene degradato e riciclato.
- Microautofagia: il lisosoma o il vacuolo ingloba direttamente piccole porzioni di citoplasma mediante invaginazione della membrana lisosomiale.
- Autofagia mediata da chaperoni: proteine solubili contenenti specifici segnali vengono riconosciute da chaperoni citosolici e trasportate direttamente attraverso la membrana lisosomiale in modo selettivo.
Meccanismi molecolari (schema semplificato della macroautofagia)
- Inizio/induzione: segnali di stress (privazione di nutrienti, differenze energetiche) inattivano il complesso regolatorio mTOR e attivano AMPK, favorendo l'attivazione del complesso ULK1 e l'avvio del processo autofilamentoso.
- Nucleazione: complessi contenenti Beclin-1 (e altri fattori) promuovono la formazione della struttura pre-autofagosomale (phagophore) e la nucleazione di membrane.
- Espansione e selezione del carico: proteine della famiglia ATG (autophagy-related genes) e la conversione di LC3-I in LC3-II favoriscono l'allungamento della membrana e l'incapsulamento del materiale destinato alla degradazione. L'autofagia può essere non selettiva (bulk) o selettiva: mitofagia (mitocondri), pexofagia (perossisomi), aggrefagia (aggregati proteici) ecc.
- Chiusura dell'autofagosoma: la membrana si chiude formando una vescicola completa a doppia membrana.
- Fusione con il lisosoma: l'autofagosoma si fonde con il lisosoma (o con un vacuolo degradativo), il contenuto viene esposto a enzimi idrolitici e degradata.
- Recupero e riciclo: prodotti della degradazione (amminoacidi, acidi grassi, zuccheri) vengono rilasciati nel citosol e riutilizzati dalla cellula.
Regolazione
L'autofagia è finemente regolata da segnali metabolici e da vie di trasduzione come:
- mTOR (mechanistic target of rapamycin): sopprime l'autofagia in condizioni di abbondanza di nutrienti.
- AMPK: sensore energetico che attiva l'autofagia in risposta a basso rapporto ATP/AMP.
- Proteine ATG, Beclin-1 e LC3: effettori diretti dell'assemblaggio della macchina autofagica.
Ruolo fisiologico e importanza biologica
L'autofagia è essenziale per:
- Mantenere la qualità degli organelli (es. mitocondri) e prevenire l'accumulo di proteine aggregate.
- Adattamento metabolico durante digiuno o stress, fornendo substrati energetici.
- Coordinare processi dello sviluppo e differenziamento cellulare e dell'omeostasi tissutale.
- Risposta immunitaria: rimuove patogeni intracellulari (xenofagia) e contribuisce alla presentazione d'antigeni.
Autofagia e malattia
Deregolazioni dell'autofagia sono associate a numerose patologie:
- Malattie neurodegenerative (Alzheimer, Parkinson, Huntington): difetti nell'autofagia favoriscono l'accumulo di proteine tossiche e la degenerazione neuronale.
- Cancro: ruolo complesso e bidirezionale — l'autofagia può prevenire l'insorgenza del tumore eliminando componenti danneggiate, ma nei tumori instaurati può aiutare cellule tumorali a sopravvivere a stress e terapie.
- Infezioni: l'autofagia può eliminare batteri e virus intracellulari, ma alcuni patogeni hanno evoluto strategie per evadere o sfruttare il processo.
- Invecchiamento e malattie metaboliche: l'efficienza dell'autofagia tende a diminuire con l'età e questo contribuisce al declino funzionale dei tessuti.
Come si studia l'autofagia
Metodi comuni includono:
- Microscopia elettronica: visualizzazione diretta degli autofagosomi.
- Marcatori biochimici: conversione di LC3-I in LC3-II, accumulo della proteina adattatrice p62/SQSTM1 (che viene degradata dall'autofagia).
- Saggi di "autophagic flux": per distinguere tra aumento della formazione di autofagosomi e blocco della degradazione (ad esempio mediante inibitori dei lisosomi come clorochina).
- Modelli genetici: delezioni o silenziamento di geni ATG nel lievito, nei modelli animali e in cellule coltivate.
Implicazioni terapeutiche
Modulare l'autofagia è un campo di grande interesse clinico. Alcuni approcci:
- Attivatori (es. inibitori di mTOR come rapamicina) possono essere utili per prevenire l'accumulo di proteine e contrastare alcune malattie neurodegenerative.
- Inibitori (es. clorochina, idrossiclorochina) bloccano la degradazione lisosomiale e sono stati sperimentati in combinazione con chemioterapie per aumentare la sensibilità delle cellule tumorali.
- La comprensione del ruolo selettivo dell'autofagia in diversi tessuti e fasi della malattia è cruciale per sviluppare terapie mirate e sicure.
Breve storia
Il termine "autofagia" è stato coniato dal biochimico belga Christian de Duve nel 1963. L'identificazione in lievito (lievito) dei geni correlati all'autofagia negli anni '90 ha permesso una rapida comprensione molecolare del processo. Questi studi hanno portato al conferimento del premio Nobel per la fisiologia o la medicina nel 2016 al ricercatore giapponese Yoshinori Ohsumi, per i suoi contributi pionieristici nello studio dell'autofagia.
In sintesi, l'autofagia è un sistema di qualità cellulare conservato evolutivamente, essenziale per la sopravvivenza, l'adattamento e la salute degli organismi. La sua modulazione rappresenta oggi una promettente strategia per trattare diverse malattie, ma richiede ancora studi approfonditi per essere sfruttata in modo sicuro ed efficace.
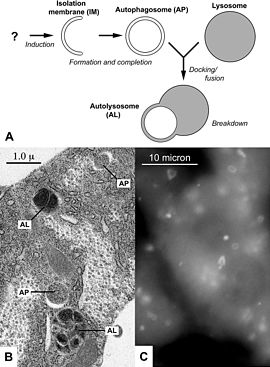
(A) Diagramma dell'autofagia; (B) Micrografia elettronica di strutture autofagiche nel corpo grasso di una larva di moscerino della frutta; (C) Autofagosomi marcati in fluorescenza in cellule epatiche di topi affamati
Domande e risposte
D: Cosa significa autofagia?
R: Autofagia significa "mangiare se stesso".
D: Qual è lo scopo dell'autofagia?
R: Lo scopo dell'autofagia è quello di consentire la rottura controllata delle parti cellulari che non funzionano o che non sono necessarie.
D: Come vengono eliminate le parti cellulari attraverso l'autofagia?
R: Le parti cellulari mirate possono essere isolate dal resto della cellula in un autofagosoma, che si fonde con i lisosomi e il contenuto viene scomposto e riciclato.
D: In quale caso estremo la rottura dei componenti cellulari promuove la sopravvivenza cellulare?
R: Nel caso estremo della fame, la disgregazione dei componenti cellulari favorisce la sopravvivenza cellulare, mantenendo i livelli di energia cellulare.
D: Chi ha coniato il termine "autofagia" e quando?
R: Il biochimico belga Christian de Duve ha coniato il termine "autofagia" nel 1963.
D: Quando sono stati identificati i geni legati all'autofagia nel lievito?
R: I geni correlati all'autofagia nel lievito sono stati identificati negli anni '90.
D: Chi ha ricevuto il Premio Nobel 2016 per la Fisiologia o la Medicina per il suo lavoro sull'autofagia?
R: Il ricercatore giapponese Yoshinori Ohsumi ha ricevuto il Premio Nobel 2016 per la Fisiologia o la Medicina per il suo lavoro sull'autofagia.
Cerca nell'enciclopedia