La legge di Boyle (chiamata anche legge di Mariotte e la legge di Boyle-Mariotte) è una legge sui gas ideali.
La legge può essere dichiarata come segue:
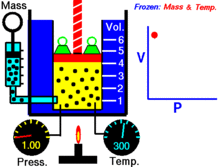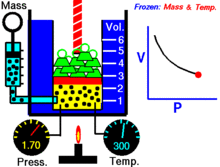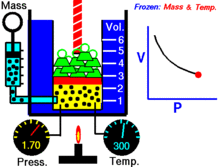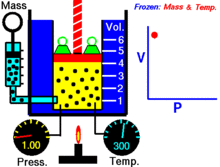
Per una quantità fissa di un gas ideale mantenuto ad una temperatura fissa, P (pressione) e V (volume) sono inversamente proporzionali.
In altre parole, il volume di una massa costante di gas ideale a temperatura costante è inversamente proporzionale alla pressione applicata su di esso.
Nei simboli, la legge è:
P ∝ 1 V {\fscx130\fscy130\frx40}P ∝ 1 V {\fscx130\fscy130\frx40}Stile P\fscy130\frx40}Propto
oppure
P V = k {\displaystyle PV=k}
dove P è la pressione del gas, V è il volume del gas, e k è una costante.
Per una data massa di gas a temperatura costante, il prodotto della pressione e del volume è una costante. Al diminuire del volume, la pressione aumenta in proporzione, e viceversa. Per esempio, quando la pressione si dimezza, il volume raddoppia.
Supponiamo di avere un serbatoio che contiene un certo volume di gas ad una certa pressione. Quando si diminuisce il volume del serbatoio, lo stesso numero di particelle di gas è ora contenuto in uno spazio più piccolo. Pertanto, il numero di collisioni aumenta. Pertanto, la pressione è maggiore.
Immaginate di avere un gas ad una certa pressione (P1) e volume (V1). Se si modifica la pressione ad un nuovo valore (P2), il volume cambia ad un nuovo valore (V2). Possiamo usare la legge di Boyle per descrivere entrambe le condizioni:
P 1 V 1 = k {\fscx130\fscy130\frx40}P 1 V 1 = k {\fscx130\fscy130\frx40}P_{1}V_{1}=k
P 2 V 2 = k {\displaystyle P_{2}V_{2}=k}
La costante, k, è la stessa in entrambi i casi, quindi possiamo dire quanto segue:
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}}=P_{2
Esempio: La pressione di un gas è di 3 atm e il volume è di 5 litri. Se la pressione è ridotta a 2 atm, qual è il volume?
P 1 V 1 = P 2 V 2 {\displaystyle P_{1}V_{1}=P_{2}V_{2}}}=P_{2
V 2 = P 1 V 1 P 2 {\displaystyle V_{2}={\frac {P_{1}V_{1}}}{P_{2}}}}
V 2 = 3 ∗ 5 2 2 {\a6}}{\a6}={\a6}{\a6}} V 2 = 3 ∗ 5
V 2 = 15 2 {\an8}{2}={\an8}}frac {15}{2}}} V 2 = 15 2 {\an8}{2}}displaystyle V_{2}==frac
V 2 = 7.5 {\a6}=7.5}=7.5
∴ Il volume sarà di 7,5 litri.
La legge fu trovata da Robert Boyle nel 1662, e poi autonomamente da Edme Mariotte nel 1679.