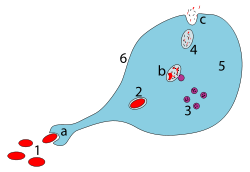
I macrofagi sono globuli bianchi all'interno dei tessuti, prodotti dalla differenziazione dei monociti.
I monociti e i macrofagi sono fagociti che agiscono nell'immunità generale. Innescono anche meccanismi di difesa specifici (immunità adattativa) dei vertebrati.
Il loro ruolo è quello di fagocitare (inghiottire e poi digerire) i detriti cellulari e gli agenti patogeni sia come cellule stazionarie che mobili. Inoltre, stimolano i linfociti e altre cellule immunitarie a rispondere all'agente patogeno,
Ai fini della chiarezza, è utile ampliare e precisare questi concetti. I macrofagi sono cellule innate estremamente versatili e presenti praticamente in tutti i tessuti (fegato, polmone, cervello, milza, ecc.). Possono derivare da monociti circolanti che migrano dal sangue ai tessuti in seguito a infiammazione, oppure possono essere popolazioni residenti stabilitesi durante lo sviluppo embrionale.
Funzioni principali:
- Fagocitosi: rimozione di batteri, virus, funghi, parassiti e detriti cellulari.
- Presentazione dell'antigene: processano antigeni e li espongono tramite molecole del complesso maggiore di istocompatibilità (MHC) per attivare i linfociti, collegando l'immunità innata a quella adattativa.
- Secrezione di mediatori: rilasciano citochine pro-infiammatorie (es. TNF-α, IL-1, IL-6) o anti-infiammatorie (es. IL-10) e chemochine che modulano la risposta immunitaria e il reclutamento di altre cellule.
- Riparazione tissutale e rimodellamento: rimuovono tessuto danneggiato e favoriscono la guarigione tramite fattori di crescita e attività di riparazione.
- Omestasi e sorveglianza: mantengono l'equilibrio nei tessuti e sorvegliano la presenza di cellule apoptotiche o trasformate.
Polarizzazione e plasticità: i macrofagi non sono una popolazione omogenea. In base ai segnali ambientali possono polarizzarsi lungo uno spettro funzionale. Due stati estremi spesso utilizzati come riferimento sono:
- M1 (classici): indotti da IFN-γ e segnali microbici; sono pro-infiammatori, bactericidi e producono alti livelli di citochine infiammatorie.
- M2 (alternativi): indotti da IL-4/IL-13 e da segnali tissutali; sono coinvolti nella risoluzione dell'infiammazione, nella riparazione e nella modulazione immunitaria.
Questa dicotomia semplifica la complessità reale, poiché i macrofagi possono assumere molteplici stati intermedi e adattarsi dinamicamente.
Macrofagi residenti e reclutati: alcuni tessuti contengono macrofagi residenti specifici con nomi particolari (es. Kupffer nel fegato, macrofagi alveolari nei polmoni, microglia nel cervello). Queste cellule spesso hanno funzioni specializzate legate all'organo in cui risiedono. In caso di infezione o danno, monociti circolanti possono differenziarsi in macrofagi reclutati che integrano la risposta locale.
Marcatori e identificazione: in laboratorio i macrofagi sono identificati con marcatori di superficie e intracellulari come CD68, CD14, CD163, oltre a uso di MHC II per la presentazione antigenica. Tuttavia i marcatori variano a seconda della specie e del tessuto.
Ruolo nelle malattie e applicazioni cliniche:
- Infiammazione cronica: il mantenimento di macrofagi pro-infiammatori può contribuire a malattie croniche come l'aterosclerosi, artrite reumatoide e malattie infiammatorie intestinali.
- Neoplasie: i macrofagi associati ai tumori (TAMs) possono sostenere la crescita tumorale, promuovere l'angiogenesi e sopprimere la risposta immunitaria antitumorale; per questo sono bersagli di terapie emergenti.
- Infezioni persistenti: alcuni patogeni evitano la distruzione intracellulare e sopravvivono all'interno dei macrofagi (es. Mycobacterium tuberculosis), rendendo la terapia più complessa.
- Terapie sperimentali: strategie comprendono la modulazione della polarizzazione (spostare da M2 a M1 nel cancro), il blocco del reclutamento, l'uso di anticorpi per la deplezione o la consegna mirata di farmaci ai macrofagi.
Durata di vita e turnover: la vita dei macrofagi varia: alcuni residenti possono durare mesi o anni, mentre quelli derivati da monociti durante l'infiammazione hanno un turnover più rapido.
Come vengono attivati: i macrofagi riconoscono agenti patogeni tramite recettori di riconoscimento (PRR) come i Toll-like receptors (TLR), che rilevano pattern molecolari associati ai patogeni (PAMP) o segnali di danno (DAMP). L'attivazione determina fagocitosi, produzione di ossido nitrico e citochine, e la presentazione antigenica.
Osservazioni finali: i macrofagi sono elementi chiave dell'immunità innata e ponti fondamentali verso l'immunità adattativa. La loro plasticità li rende indispensabili per la difesa, la riparazione e la regolazione dell'omeostasi tissutale, ma la loro disfunzione può contribuire a molte malattie. Comprendere i segnali che ne guidano la funzione è essenziale per sviluppare terapie mirate.