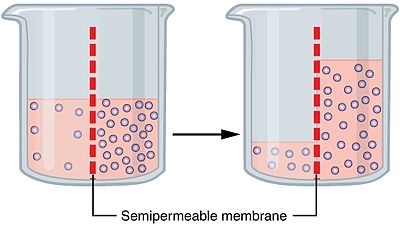
Osmosi indica il movimento spontaneo del solvente — spesso l'acqua — attraverso una membrana semipermeabile, che lascia passare il solvente ma ostacola i soluti. Il flusso avviene in modo da ridurre la differenza di concentrazione tra i due lati della membrana: il solvente si sposta verso la regione a maggior concentrazione di soluto, tendendo ad equalizzare le differenze di concentrazione. L'osmosi è un processo di trasporto passivo e la sua intensità dipende dalla differenza di energia chimica (o potenziale) del solvente ai due lati della membrana.
Meccanismo e direzione del flusso
Il fenomeno è guidato dal gradiente chimico del solvente: il movimento avviene da una regione con minore concentrazione di soluto (quindi maggiore presenza di solvente libero) verso una regione con maggiore concentrazione di soluto. In pratica, l'acqua si muove per compensare la differenza di attività chimica del solvente; questa tendenza può essere contrastata da una pressione esterna applicata contro il flusso.
Pressione osmotica
La pressione osmotica è la pressione esterna minima da applicare al lato più concentrato per annullare il flusso osmotico. Per soluzioni idealmente diluite la pressione osmotica è approssimativamente proporzionale alla concentrazione molare dei soluti (legge di van ’t Hoff), ma in soluzioni reali possono intervenire deviazioni dovute a interazioni tra particelle.
Tonicità e conseguenze per le cellule
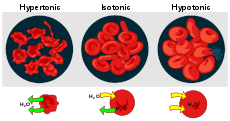
La tonicità descrive l'effetto di una soluzione sul volume cellulare tramite osmosi. In termini generali:
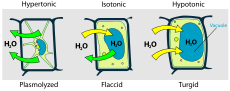
- Soluzione ipotonica: concentrazione di soluto esterna inferiore rispetto all'interno della cellula → ingresso di acqua, possibile rigonfiamento o lisi.
- Soluzione ipertonica: concentrazione esterna maggiore → uscita di acqua, possibile plasmolisi o disidratazione cellulare.
- Soluzione isotonica: equilibrio di volume netto, nessun flusso netto di solvente.
Un esempio concreto del fenomeno è il movimento di molecole di liquido (solvente) attraverso una membrana cellulare quando la cellula è immersa in un mezzo con una concentrazione di soluto diversa. L'osmosi è quindi centrale nella biochimica e nella fisiologia cellulare.
Importanza biologica e applicazioni pratiche
- Negli organismi vegetali, la pressione di turgore ottenuta per osmosi mantiene la rigidezza delle cellule e il sostegno delle piante.
- Negli animali, l'equilibrio osmotico tra sangue e liquidi extracellulari è essenziale per la funzione cellulare e per il volume plasmatico.
- In medicina, processi basati sull'osmosi sono alla base di terapie come la dialisi peritoneale e di apparecchiature per la purificazione dei liquidi biologici.
- In ingegneria e trattamento acque, la osmosi inversa è impiegata per la desalinizzazione e la rimozione di impurità dall'acqua.
Osservazioni sperimentali e limiti
Misurare la pressione osmotica o il flusso di solvente richiede strumenti specifici (osmometri, celle a membrana) e condizioni controllate: temperatura, natura del soluto, permeabilità della membrana e non idealità della soluzione influenzano i risultati. In sistemi complessi, come le membrane biologiche, intervengono inoltre trasportatori e canali che possono modificare il comportamento osservato rispetto al caso ideale.
Concetti correlati
- Membrana semipermeabile: barriera che consente il passaggio del solvente ma non di certi soluti.
- Gradiente chimico: differenza di energia chimica che guida il movimento delle molecole.
- Equilibrio osmotico: condizione nella quale non c'è più flusso netto di solvente attraverso la membrana.
Per approfondire i singoli aspetti sperimentali o applicativi, si consiglia di consultare testi specialistici di fisiologia cellulare, biochimica e ingegneria dei processi di separazione.