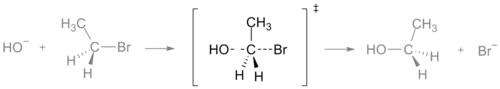In una reazione chimica, lo stato di transizione è il punto in cui c'è un valore massimo di energia. Questa energia è chiamata energia di attivazione. Quando due o più molecole si mescolano, si colpiscono a vicenda. Se si scontrano con abbastanza energia da passare attraverso lo stato di transizione, reagiranno e formeranno nuove molecole. Allo stato di transizione, si formano nuovi legami mentre quelli vecchi si rompono. In un grafico o in un disegno, lo stato di transizione è spesso segnato con il simbolo del doppio pugnale ‡.
È molto difficile studiare uno stato di transizione. Questo perché è così alto in energia che le molecole rimarranno in quella forma per un tempo molto breve, di solito femtosecondi. È importante non confondere gli stati di transizione con gli intermedi. Gli intermedi si trovano in punti minimi di energia, e possono vivere per un tempo molto lungo. Come uno stato di transizione, tuttavia, un intermedio si trova tra i reagenti e i prodotti di una reazione.
Lo studio degli stati di transizione è molto importante per capire i meccanismi di reazione. Ci sono teorie e programmi per computer che possono essere usati per calcolare l'aspetto dello stato di transizione. Questa è una parte della cinetica chimica.