Reazione chimica
Una reazione chimica avviene quando una o più sostanze chimiche vengono trasformate in una o più altre sostanze chimiche. Esempi:
- ferro e ossigeno che si combinano per formare la ruggine
- aceto e bicarbonato di sodio che si combinano per ottenere acetato di sodio, anidride carbonica e acqua
- cose che bruciano o esplodono
- molte reazioni che avvengono all'interno degli esseri viventi
- reazioni elettrochimiche durante la scarica o la ricarica delle batterie
Alcune reazioni sono veloci, altre lente. Alcune avvengono a velocità diverse, a seconda della temperatura o di altre cose. Per esempio, il legno non reagisce con l'aria quando è freddo, ma se è reso abbastanza caldo, inizierà a bruciare. Alcune reazioni emettono energia. Si tratta di reazioni esotermiche. In altre reazioni l'energia viene assorbita. Queste sono reazioni endotermiche.
Le reazioni nucleari non sono reazioni chimiche. Le reazioni chimiche coinvolgono solo gli elettroni degli atomi; le reazioni nucleari coinvolgono i protoni e i neutroni nei nuclei atomici.

Ferro arrugginito

Un falò è un esempio di redox
Quattro tipi di base
Sintesi
In una reazione di sintesi, due o più sostanze semplici si combinano per formare una sostanza più complessa.
A + B ⟶ A B {\fscx130\fscy130\frx40}A+B
"Due o più reagenti che danno un prodotto" è un altro modo per identificare una reazione di sintesi. Un esempio di reazione di sintesi è la combinazione di ferro e zolfo per formare il solfuro di ferro (II):
8 F e + S 8 ⟶ 8 F e S {\displaystyle 8Fe+S_{8}\longrightarrow 8FeS} {longrowarrow 8FeS}
Un altro esempio è il semplice gas idrogeno combinato con il semplice gas ossigeno per produrre una sostanza più complessa, come l'acqua.
Decomposizione
Una reazione di decomposizione è quando una sostanza più complessa si scompone nelle sue parti più semplici. È quindi l'opposto di una reazione di sintesi, e può essere scritto come:
A B ⟶ A + B {\fscx130\fscy130\frx40}A B ⟶ A + B {\fscx130\fscy130\frx40}A + B
Un esempio di reazione di decomposizione è l'elettrolisi dell'acqua per produrre ossigeno e idrogeno gassoso:
2 H 2 O ⟶ 2 H 2 + O 2 {\fscx130\fscy130\frx40}O{2}O{2}O{2}+O_{2}}}Stile di visualizzazione 2H_{2}O {\fscx130\fscy130\frx40}O{2
Sostituzione singola
In una singola reazione di sostituzione, un singolo elemento non combinato ne sostituisce un altro in un composto; in altre parole, un elemento viene scambiato con un altro elemento in un composto:
A + B C ⟶ A C + B {\fscx130\fscy130\fscy130\frx40}A + B ⟶ A C + B {\fscx130\fscy130\frx40}A+B
Un esempio di reazione a singolo spostamento è quando il magnesio sostituisce l'idrogeno nell'acqua per produrre idrossido di magnesio e idrogeno gassoso:
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\fscx130\fscy130\frx40}O\fscy130\frx40}M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\fscx130\fscy130\frx40}Mg+2H_{2}O\fscy130\frx40}O
Doppia sostituzione
In una doppia reazione di sostituzione, gli anioni e i cationi di due composti si scambiano di posto e formano due composti completamente diversi. Queste reazioni sono nella forma generale:
A B + C D ⟶ A D + C C B {\displaystyle AB+CD\fscx130\fscy130\fscy130\frx40}A B + C D ⟶ A D + C B
Per esempio, quando il cloruro di bario (BaCl2) e il solfato di magnesio (MgSO4) reagiscono, l'anione SO42- si commuta con l'anione 2Cl-, dando ai composti BaSO4 e MgCl2.
Un altro esempio di reazione a doppio spostamento è la reazione del nitrato di piombo (II) con ioduro di potassio per formare ioduro di piombo (II) e nitrato di potassio:
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}}}
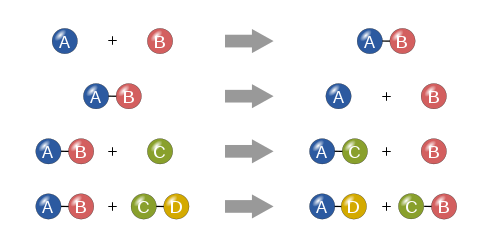
I quattro tipi di reazioni chimiche di base: sintesi, decomposizione, sostituzione singola e doppia sostituzione
Equazioni
Una reazione chimica viene visualizzata da un'equazione:
A + B ⟶ ⟶ C + D {\an8}Mathrm {A+B {A+B \an8}C + D }
Qui, A e B reagiscono a C e D in una reazione chimica.
Questo è un esempio di reazione di combustione.
C + O 2 ⟶ C O 2 \displaystyle \mathrm {C+O_{2} {C+O_{2} {\an8}longrightarrow CO_{2}}} }
Pagine correlate
- Reazione organica
- Redox
Domande e risposte
D: Che cos'è una reazione chimica?
R: Una reazione chimica avviene quando una o più sostanze chimiche si trasformano in una o più altre sostanze chimiche.
D: Può fare degli esempi di reazioni chimiche?
R: Sì, alcuni esempi di reazioni chimiche sono il ferro e l'ossigeno che si combinano per formare la ruggine, l'aceto e il bicarbonato di sodio che si combinano per formare l'acetato di sodio, l'anidride carbonica e l'acqua, le cose che bruciano o esplodono e molte reazioni che avvengono all'interno degli esseri viventi, come la fotosintesi.
D: Tutte le reazioni chimiche sono veloci?
R: No, alcune reazioni sono veloci e altre sono lente. Alcune avvengono a velocità diverse, a seconda della temperatura o di altri fattori.
D: Che cos'è una reazione esotermica?
R: Una reazione esotermica è una reazione che cede energia.
D: Che cos'è una reazione endotermica?
R: Una reazione endotermica è una reazione che assorbe energia.
D: Le reazioni nucleari sono considerate reazioni chimiche?
R: No, le reazioni nucleari non sono reazioni chimiche. Le reazioni chimiche coinvolgono solo gli elettroni degli atomi; le reazioni nucleari coinvolgono i protoni e i neutroni nei nuclei atomici.
D: La temperatura può influenzare la velocità di una reazione chimica?
R: Sì, a seconda della temperatura o di altri fattori, alcune reazioni possono avvenire a velocità diverse. Ad esempio, il legno non reagisce con l'aria quando è freddo, ma se viene reso abbastanza caldo, inizierà a bruciare.
Cerca nell'enciclopedia









