In chimica, le forze di van der Waals sono un tipo di forza intermolecolare. Una forza intermolecolare è una forza relativamente debole che tiene insieme le molecole. Le forze di Van der Waals sono il tipo più debole di forza intermolecolare. Prendono il nome dallo scienziato olandese Johannes Diderik van der Waals (1837-1923).
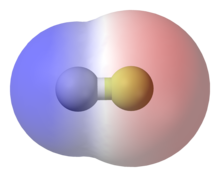
Gli elettroni carichi negativamente orbitano in molecole o ioni. Gli elettroni creano cariche leggermente diverse da un'estremità all'altra della molecola. Queste leggere differenze sono chiamate cariche parziali, come δ- o δ+.
Il termine è a volte usato vagamente come sinonimo di tutte le forze intermolecolari. Le forze di Van der Waals sono relativamente deboli rispetto ai legami covalenti, ma svolgono un ruolo fondamentale nella chimica supramolecolare, negli enzimi, nella scienza dei polimeri, nella nanotecnologia, nella scienza delle superfici e nella fisica della materia condensata. Le forze di Van der Waals definiscono molte proprietà dei composti organici, compresa la loro solubilità.

