Gli enzimi sono molecole proteiche presenti nelle cellule che funzionano come catalizzatori biologici. Gli enzimi accelerano le reazioni chimiche nel corpo senza consumarsi nel processo, perciò possono essere utilizzati ripetutamente.
Quasi tutte le reazioni biochimiche negli esseri viventi richiedono enzimi. In loro presenza, le reazioni procedono molto più rapidamente rispetto a quanto avverrebbe senza un catalizzatore proteico. p39 Oltre alle proteine enzimatiche, esistono anche biocatalizzatori di natura diversa, come le molecole di RNA catalitiche, dette ribozimi, che possono svolgere attività simili in alcuni processi cellulari.
Struttura e meccanismo d'azione
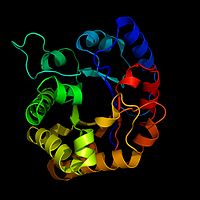
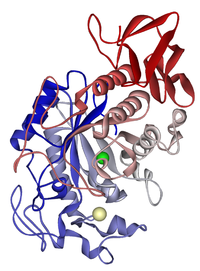
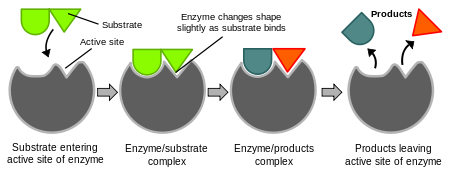
La maggior parte degli enzimi è costituita da una catena di amminoacidi ripiegata in una struttura tridimensionale specifica. In questa struttura si trova il sito attivo, una regione del proteinà dove il substrato si lega. Il sito attivo è modellato in modo da riconoscere il substrato e stabilizzare lo stato di transizione della reazione, abbassando l'energia necessaria per avviare la reazione.
Due modelli utili per comprendere il legame enzima-substrato sono il modello "chiave-serratura" e il modello dell'induced fit (adattamento indotto). Nel primo il sito attivo è complementare al substrato; nel secondo l'enzima cambia leggermente forma al momento del legame per ottimizzare l'interazione.
Molti enzimi richiedono elementi non proteici per funzionare correttamente:
- Cofattori: ioni metallici (es. Mg2+, Fe2+) o gruppi prostetici.
- Coenzimi: molecole organiche (spesso derivate da vitamine) che trasportano gruppi chimici o elettroni (es. NAD+, FAD).
Specificità e classificazione
Gli enzimi sono specifici: riconoscono uno o pochi substrati e catalizzano reazioni precise. Molti enzimi hanno nomi che finiscono in -asi (es. amilasi, lattasi). Per motivi pratici esiste anche una classificazione internazionale (numero EC) che suddivide gli enzimi in classi principali, ad esempio:
- ossidoriduttasi (ossidoriduzioni)
- transferasi (trasferimento di gruppi)
- idrolasi (rottura mediante acqua)
- lisi (addizione o rimozione di gruppi senza acqua)
- isomerasi (isomerizzazioni)
- ligasi (formazione di legami con consumo di ATP)
Fattori che influenzano l'attività enzimatica
L'attività di un enzima dipende da vari fattori esterni e interni:
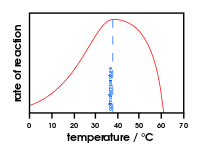
- Temperatura: ogni enzima ha una temperatura ottimale; temperature troppo alte possono denaturare la proteina.
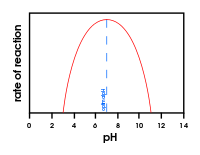
- pH: anche il pH ottimale varia tra enzimi e influisce sulla carica degli amminoacidi nel sito attivo.
- Concentrazione di substrato: all'aumentare del substrato la velocità aumenta fino a un plateau (saturazione).
- Inibitori: sostanze che riducono l'attività enzimatica. Possono essere competitivi (si legano al sito attivo) o non competitivi/allosterici (si legano altrove e modificano la funzione).
- Attivatori e modificazioni covalenti: alcuni enzimi sono attivati o inattivati da legame di piccoli effettori o da modificazioni come la fosforilazione.
Ruolo nelle reazioni biologiche e nella regolazione metabolica
Gli enzimi coordinano i percorsi metabolici che trasformano nutrienti in energia e componenti cellulari. Agiscono in sequenze organizzate (vie metaboliche) e la loro regolazione assicura che la cellula risponda ai cambiamenti ambientali e alle necessità energetiche. Meccanismi di controllo comuni sono:
- Inibizione da feedback: il prodotto finale di una via inibisce un enzima iniziale della stessa via.
- Controllo allosterico: effettori si legano a siti diversi dal sito attivo cambiando l'attività enzimatica.
- Modificazioni post-traduzionali: es. fosforilazione/de-fosforilazione per attivare o disattivare rapidamente un enzima.
Esempi e applicazioni pratiche
Esempi comuni di enzimi includono: la amilasi (digestione dei carboidrati), la lattasi (scissione del lattosio), le DNA polimerasi (replicazione del materiale genetico) e l'ATP sintasi (sintesi di ATP). Le applicazioni pratiche sono numerose:
- Medicina: molti farmaci agiscono su enzimi; test diagnostici misurano attività enzimatiche; terapie enzimatiche per carenze specifiche.
- Industria alimentare: enzimi usati nella produzione di formaggi, birra, pane e nella chiarificazione dei succhi.
- Biotecnologie: enzimi termostabili (es. Taq polimerasi) sono essenziali per tecniche come la PCR.
- Detergenti e biocatalisi: enzimi proteolitici, lipasici e amilasici migliorano l'efficacia dei detergenti e sono usati per reazioni chimiche più sostenibili.
Breve cenno storico
Il primo enzima isolato fu scoperto nel 1833 da Anselme Payen, che identificò la "diastasi" (oggi nota come amilasi). Il termine "enzima" e la comprensione moderna delle loro funzioni si sono sviluppati nei decenni successivi grazie ai progressi in chimica e biologia molecolare.
Lo studio approfondito degli enzimi è noto come enzimologia: disciplina fondamentale per comprendere la vita, sviluppare terapie e progettare processi biotecnologici.