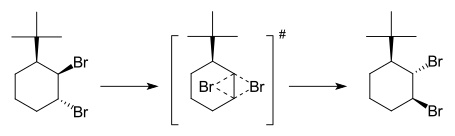
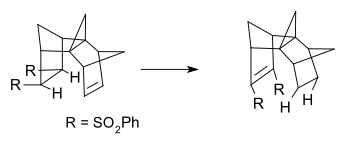
Una reazione disotropa è un tipo di reazione chimica. È quando un composto organico cambia la sua struttura. Due sostituti saltano da un punto della molecola ad un altro. È una isomerizzazione di valenza periciclica quando due legami sigma si spostano contemporaneamente in un nuovo posto sulla stessa molecola. Le reazioni disotrope sono importanti nella chimica organica. Possono spiegare come funzionano certe reazioni. Le reazioni disotrope possono essere un passo utile nella realizzazione di molecole grandi e complicate. Le reazioni disotrope sono state descritte per la prima volta da Manfred T. Reetz nel 1971. Il nome "reazione disotropa" deriva dalla parola greca dyo che significa "due". "Riordinamento" significa che la reazione cambia i legami tra gli atomi su una singola molecola.
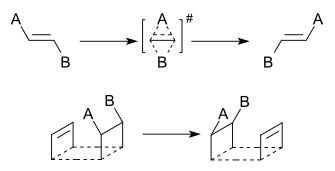
In una reazione di tipo I, due gruppi di migranti scambiano le loro posizioni relative. Una reazione di tipo II comporta la migrazione verso nuovi siti di legame senza scambio di posizioni.