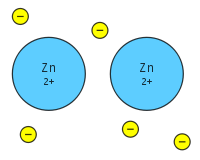
Un legame metallico è la condivisione di molti elettroni staccati tra molti ioni positivi, dove gli elettroni agiscono come "colla" dando alla sostanza una struttura definita. È diverso dal legame covalente o ionico. I metalli hanno una bassa energia di ionizzazione. Pertanto, gli elettroni di valenza possono essere delocalizzati in tutti i metalli. Gli elettroni delocalizzati non sono associati ad un particolare nucleo di un metallo, ma sono liberi di muoversi attraverso l'intera struttura cristallina formando un "mare" di elettroni.
Gli elettroni e gli ioni positivi nel metallo hanno una forte forza attrattiva tra loro. Pertanto, i metalli hanno spesso un alto punto di fusione o di ebollizione. Il principio è simile a quello dei legami ionici.
I legami metallici causano molti dei tratti dei metalli, come la resistenza, la malleabilità, la duttilità, la lucentezza, la conduzione del calore e dell'elettricità.
Poiché gli elettroni si muovono liberamente, il metallo ha una certa conducibilità elettrica. Permette all'energia di passare rapidamente attraverso gli elettroni, generando una corrente elettrica. I metalli conducono il calore per lo stesso motivo: gli elettroni liberi possono trasferire l'energia ad un ritmo più veloce rispetto ad altre sostanze con elettroni fissati in posizione. Ci sono anche pochi non-metalli che conducono l'elettricità: la grafite (perché, come i metalli, ha elettroni liberi), e i composti ionici che sono fusi o sciolti in acqua, che hanno ioni liberi in movimento.
I legami metallici hanno almeno un elettrone di valenza che non condividono con gli atomi vicini e non perdono elettroni per formare ioni. Al contrario, i livelli di energia esterna (orbite atomiche) degli atomi metallici si sovrappongono. Sono simili ai legami covalenti. Non tutti i metalli presentano legami metallici. Ad esempio, gli ioni di mercurio (Hg2+
2) formare legami metallo-metallo covalenti.
Una lega è una soluzione di metalli. La maggior parte delle leghe sono lucide come lo sono i metalli puri.