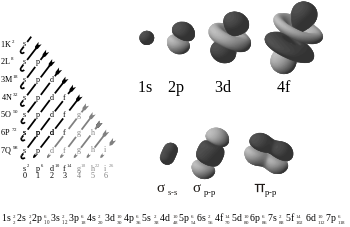
In chimica, i legami pi greco (legami π) sono legami chimici covalenti in cui il percorso orbitale di un elettrone si incrocia (si sovrappone) con il percorso di un altro elettrone. Gli elettroni hanno una figura a lobi di otto percorsi (vedi figura). Ci sono due aree di sovrapposizione in quanto i percorsi si sovrappongono su entrambi i lobi. Solo uno dei piani nodali dell'orbita passa attraverso entrambi i nuclei coinvolti.
La lettera greca π nel loro nome si riferisce agli orbitali p. La simmetria orbitale del legame pi greco ha lo stesso aspetto dell'orbitale p se vista lungo l'asse del legame. Le orbite p hanno di solito questo tipo di legame. Anche gli orbitali D si suppone che utilizzino il legame pi, ma questo non è necessariamente ciò che accade nella realtà. L'idea del legame degli orbitali d si adatta alla teoria dell'ipervigilanza.
I Pi bond sono di solito più deboli dei sigma bond. La meccanica quantistica dice che questo è dovuto al fatto che i percorsi orbitali sono paralleli, quindi c'è molta meno sovrapposizione tra i p-orbitali.
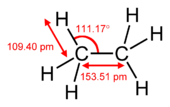
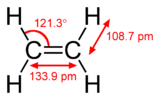
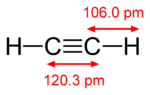
I legami Pi si verificano quando due orbite atomiche sono in contatto attraverso due aree di sovrapposizione. I Pi-bond sono legami più spalmati rispetto ai sigma bond. Gli elettroni nei legami pi greco sono talvolta chiamati elettroni pi greco. I frammenti molecolari uniti da un legame pi greco non possono ruotare intorno a quel legame senza rompere il legame pi greco. La rotazione distrugge i percorsi paralleli dei due p orbitali.