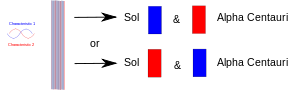
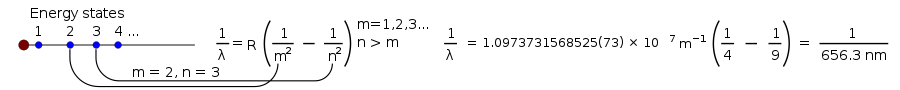Le formule e le idee della meccanica quantistica furono fatte per spiegare la luce che proviene dall'idrogeno incandescente. La teoria quantistica dell'atomo doveva anche spiegare perché l'elettrone rimane nella sua orbita, cosa che altre idee non erano in grado di spiegare. In base alle idee più vecchie, l'elettrone avrebbe dovuto cadere verso il centro dell'atomo perché all'inizio era tenuto in orbita dalla sua stessa energia, ma avrebbe perso rapidamente la sua energia mentre girava nella sua orbita. (Questo perché si sapeva che gli elettroni e altre particelle cariche emettono luce e perdono energia quando cambiano velocità o girano).
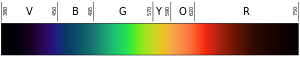
Le lampade a idrogeno funzionano come le luci al neon, ma le luci al neon hanno il loro gruppo unico di colori (e frequenze) di luce. Gli scienziati hanno imparato che potevano identificare tutti gli elementi dai colori della luce che producono. Solo che non riuscivano a capire come venivano determinate le frequenze.
Poi, un matematico svizzero di nome Johann Balmer scoprì un'equazione che diceva quale sarebbe stato λ (lambda, per la lunghezza d'onda):
λ = B ( n 2 n 2 - 4 ) n = 3 , 4 , 5 , 6 {\displaystyle \lambda =B\left({\frac {n^{2}}{n^{2}-4}}} destra)\qquad \qquad n=3,4,5,6} 
dove B è un numero che Balmer ha determinato essere uguale a 364,56 nm.
Questa equazione funzionava solo per la luce visibile di una lampada a idrogeno. Ma più tardi, l'equazione fu resa più generale:
1 λ = R ( 1 m 2 - 1 n 2 ) , {displaystyle {{frac {1}{lambda }}=R\sinistra({frac {1}{m^{2}}}-{frac {1}{n^{2}}} destra),} 
dove R è la costante di Rydberg, pari a 0,0110 nm-1, e n deve essere maggiore di m.
Mettendo diversi numeri per m e n, è facile prevedere le frequenze per molti tipi di luce (ultravioletta, visibile e infrarossa). Per vedere come funziona, vai su Hyperphysics e vai giù oltre il centro della pagina. (Usa H = 1 per l'idrogeno).
Nel 1908, Walter Ritz realizzò il principio di combinazione di Ritz che mostra come certi intervalli tra le frequenze continuano a ripetersi. Questo si rivelò importante per Werner Heisenberg diversi anni dopo.
Nel 1905, Albert Einstein utilizzò l'idea di Planck per dimostrare che un raggio di luce è composto da un flusso di particelle chiamate fotoni. L'energia di ogni fotone dipende dalla sua frequenza. L'idea di Einstein è l'inizio dell'idea della meccanica quantistica che tutte le particelle subatomiche come elettroni, protoni, neutroni e altri sono onde e particelle allo stesso tempo. (Vedi l'immagine dell'atomo con l'elettrone come onda nell'atomo). Questo ha portato a una teoria sulle particelle subatomiche e le onde elettromagnetiche chiamata dualità onda-particella. Questo è dove le particelle e le onde non erano né l'una né l'altra, ma avevano certe proprietà di entrambe.
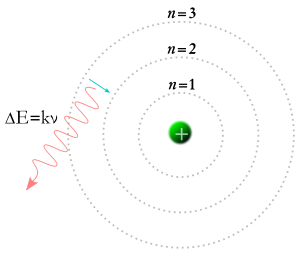
Nel 1913, Niels Bohr ebbe l'idea che gli elettroni potessero occupare solo certe orbite intorno al nucleo di un atomo. Secondo la teoria di Bohr, i numeri chiamati m e n nell'equazione sopra potrebbero rappresentare delle orbite. La teoria di Bohr diceva che gli elettroni potevano iniziare in una certa orbita m e finire in una certa orbita n, o un elettrone poteva iniziare in una certa orbita n e finire in una certa orbita m, quindi se un fotone colpisce un elettrone, la sua energia sarà assorbita e l'elettrone si sposterà in un'orbita superiore a causa di quell'energia extra. Secondo la teoria di Bohr, se un elettrone cade da un'orbita superiore a un'orbita inferiore, allora dovrà cedere energia sotto forma di un fotone. L'energia del fotone sarà uguale alla differenza di energia tra le due orbite, e l'energia di un fotone gli fa avere una certa frequenza e colore. La teoria di Bohr forniva una buona spiegazione di molti aspetti dei fenomeni subatomici, ma non riusciva a rispondere al perché ciascuno dei colori della luce prodotta dall'idrogeno incandescente (e dal neon incandescente o da qualsiasi altro elemento) ha una luminosità propria, e le differenze di luminosità sono sempre le stesse per ogni elemento.
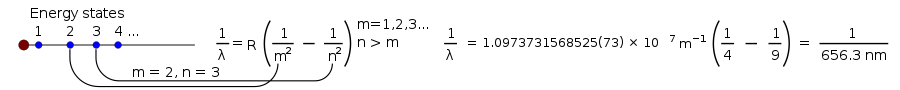
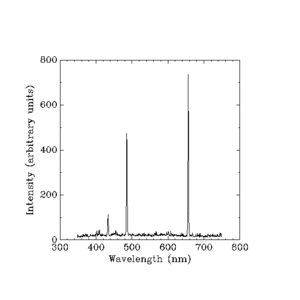
Quando Niels Bohr presentò la sua teoria, la maggior parte delle cose sulla luce prodotta da una lampada a idrogeno erano note, ma gli scienziati non riuscivano ancora a spiegare la luminosità di ciascuna delle linee prodotte dall'idrogeno incandescente.
Werner Heisenberg si incaricò di spiegare la luminosità o "intensità" di ogni linea. Non poteva usare nessuna regola semplice come quella di Balmer. Dovette usare la matematica molto difficile della fisica classica che calcola tutto in termini di cose come la massa (peso) di un elettrone, la carica (forza elettrica statica) di un elettrone e altre piccole quantità. La fisica classica aveva già delle risposte per la luminosità delle bande di colore che una lampada a idrogeno produce, ma la teoria classica diceva che ci doveva essere un arcobaleno continuo, e non quattro bande di colore separate. La spiegazione di Heisenberg è:
C'è una legge che dice quali frequenze di luce l'idrogeno incandescente produrrà. Deve prevedere frequenze distanziate quando gli elettroni coinvolti si muovono tra orbite vicine al nucleo (centro) dell'atomo, ma deve anche prevedere che le frequenze si avvicineranno sempre di più man mano che osserviamo ciò che l'elettrone fa nel muoversi tra orbite sempre più lontane. Prevede anche che le differenze di intensità tra le frequenze si avvicinano sempre di più man mano che ci allontaniamo. Dove la fisica classica dà già le risposte giuste con una serie di equazioni, la nuova fisica deve dare le stesse risposte ma con equazioni diverse.
La fisica classica usa i metodi del matematico francese Fourier per fare un'immagine matematica del mondo fisico, e usa collezioni di curve lisce che vanno insieme per fare una curva liscia che dà, in questo caso, intensità per la luce di tutte le frequenze da una certa luce. Ma non è giusto perché quella curva liscia appare solo a frequenze più alte. Alle frequenze più basse, ci sono sempre punti isolati e niente collega i punti. Così, per fare una mappa del mondo reale, Heisenberg ha dovuto fare un grande cambiamento. Doveva fare qualcosa per scegliere solo i numeri che corrispondessero a ciò che si vedeva in natura. A volte la gente dice che ha "indovinato" queste equazioni, ma non stava facendo congetture alla cieca. Ha trovato ciò che gli serviva. I numeri che calcolava mettevano dei punti su un grafico, ma non c'era nessuna linea tracciata tra i punti. E fare un "grafico" solo di punti per ogni serie di calcoli avrebbe sprecato molta carta e non avrebbe ottenuto nulla. Heisenberg ha trovato un modo per prevedere in modo efficiente le intensità per diverse frequenze e per organizzare queste informazioni in modo utile.
Solo usando la regola empirica data sopra, quella che Balmer ha iniziato e Rydberg ha migliorato, possiamo vedere come ottenere una serie di numeri che aiuterebbero Heisenberg a ottenere il tipo di immagine che voleva:
La regola dice che quando l'elettrone si sposta da un'orbita all'altra, guadagna o perde energia, a seconda che si stia allontanando dal centro o avvicinando ad esso. Così possiamo mettere queste orbite o livelli di energia come titoli lungo la parte superiore e laterale di una griglia. Per ragioni storiche l'orbita più bassa si chiama n, e l'orbita successiva si chiama n - a, poi viene n - b, e così via. È confuso il fatto che abbiano usato numeri negativi quando gli elettroni stavano effettivamente guadagnando energia, ma questo è solo il modo in cui è.
Poiché la regola di Rydberg ci dà delle frequenze, possiamo usare questa regola per mettere dei numeri a seconda di dove va l'elettrone. Se l'elettrone parte da n e finisce a n, allora non è andato da nessuna parte, quindi non ha guadagnato e non ha perso energia. Quindi la frequenza è 0. Se l'elettrone parte da n-a e finisce a n, allora è caduto da un'orbita superiore a un'orbita inferiore. Se lo fa, allora perde energia, e l'energia che perde si presenta come un fotone. Il fotone ha una certa quantità di energia, e, che è legata a una certa frequenza f dall'equazione e = h f. Quindi sappiamo che un certo cambiamento di orbita produrrà una certa frequenza della luce, f. Se l'elettrone parte da n e finisce a n - a, significa che è passato da un'orbita inferiore a un'orbita superiore. Questo accade solo quando un fotone di una certa frequenza ed energia arriva dall'esterno, viene assorbito dall'elettrone e gli dà la sua energia, e questo è ciò che fa uscire l'elettrone verso un'orbita superiore. Quindi, per dare un senso a tutto, scriviamo quella frequenza come un numero negativo. C'era un fotone con una certa frequenza e ora è stato portato via.
Quindi possiamo fare una griglia come questa, dove f(a←b) indica la frequenza coinvolta quando un elettrone passa dallo stato energetico (orbita) b allo stato energetico a (di nuovo, le sequenze sembrano al contrario, ma questo è il modo in cui sono state scritte originariamente):
Griglia di f
| Stati dell'elettrone | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| transizione .... | ..... | ..... | ..... | ..... | | |
Heisenberg non ha fatto le griglie in questo modo. Ha solo fatto i calcoli che gli avrebbero permesso di ottenere le intensità che stava cercando. Ma per farlo doveva moltiplicare due ampiezze (quanto alta misura un'onda) per calcolare l'intensità. (Nella fisica classica, l'intensità è uguale all'ampiezza al quadrato). Fece una strana equazione per gestire questo problema, scrisse il resto del suo documento, lo consegnò al suo capo e andò in vacanza. Il dottor Born guardò la sua strana equazione e gli sembrò un po' folle. Deve essersi chiesto: "Perché Heisenberg mi ha dato questa cosa strana? Perché deve fare così?". Poi si rese conto che stava guardando un progetto di qualcosa che conosceva già molto bene. Era abituato a chiamare matrice la griglia o la tabella che potevamo scrivere facendo, per esempio, tutta la matematica delle frequenze. E la strana equazione di Heisenberg era una regola per moltiplicarne due insieme. Max Born era un matematico molto, molto bravo. Sapeva che poiché le due matrici (griglie) che venivano moltiplicate rappresentavano cose diverse (come la posizione (x,y,z) e la quantità di moto (mv), per esempio), allora quando si moltiplica la prima matrice per la seconda si ottiene una risposta e quando si moltiplica la seconda matrice per la prima matrice si ottiene un'altra risposta. Anche se non conosceva la matematica delle matrici, Heisenberg aveva già visto questo problema delle "risposte diverse" e lo aveva infastidito. Ma il dottor Born era un matematico così bravo che vide che la differenza tra la prima moltiplicazione della matrice e la seconda moltiplicazione della matrice coinvolgeva sempre la costante di Planck, h, moltiplicata per la radice quadrata di uno negativo, i. Così in pochi giorni dalla scoperta di Heisenberg avevano già la matematica di base per quello che Heisenberg amava chiamare il "principio di indeterminazione". Con "indeterminato" Heisenberg intendeva che qualcosa come un elettrone non è semplicemente inchiodato finché non viene inchiodato. È un po' come una medusa che è sempre in giro e non può stare "in un posto" a meno che non la si uccida. Più tardi, la gente ha preso l'abitudine di chiamarlo "principio di indeterminazione di Heisenberg", che ha fatto commettere a molte persone l'errore di pensare che gli elettroni e cose del genere siano davvero "da qualche parte" ma che siamo solo incerti nella nostra mente. Questa idea è sbagliata. Non è quello di cui parlava Heisenberg. Avere problemi a misurare qualcosa è un problema, ma non è il problema di cui parlava Heisenberg.
L'idea di Heisenberg è molto difficile da afferrare, ma possiamo renderla più chiara con un esempio. Per prima cosa, inizieremo a chiamare queste griglie "matrici", perché presto avremo bisogno di parlare di moltiplicazione di matrici.
Supponiamo di iniziare con due tipi di misure, posizione (q) e quantità di moto (p). Nel 1925, Heisenberg scrisse un'equazione come questa:
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\displaystyle Y(n,n-b)=\sum _{a}^{\},p(n,n-a)q(n-a,n-b)}  (Equazione per le variabili coniugate quantità di moto e posizione)
(Equazione per le variabili coniugate quantità di moto e posizione)
Lui non lo sapeva, ma questa equazione fornisce un modello per scrivere due matrici (griglie) e per moltiplicarle. Le regole per moltiplicare una matrice per un'altra sono un po' confuse, ma ecco le due matrici secondo lo schema, e poi il loro prodotto:
Matrice di p
| Stati dell'elettrone | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| transizione .... | ..... | ..... | ..... | ..... | |
Matrice di q
| Stati dell'elettrone | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| transizione .... | ..... | ..... | ..... | ..... | |
La matrice per il prodotto delle due matrici di cui sopra, come specificato dalla relativa equazione nel documento di Heisenberg del 1925, è:
| Stati dell'elettrone | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Dove:
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+ .....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+ .....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+ .....
e così via.
Se le matrici fossero invertite, si otterrebbero i seguenti valori:
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b)+.....
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c)+.....
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+ .....
e così via.
Nota come cambiare l'ordine di moltiplicazione cambia i numeri, passo dopo passo, che vengono effettivamente moltiplicati.