La cristallografia a raggi X è una tecnica sperimentale usata per determinare la struttura tridimensionale di molecole e solidi a livello atomico. Quando un fascio di raggi X interagisce con la nube di elettroni intorno agli atomi, i raggi vengono deviati e interferiscono tra loro: il risultato è un pattern di diffrazione che, opportunamente analizzato, fornisce una mappa della densità elettronica e quindi la posizione degli atomi nella struttura. Questa tecnica è applicabile sia a sistemi organici sia a composti inorganici; in genere il campione non viene completamente distrutto dall'esperimento, anche se è importante ricordare che l’irraggiamento può provocare danni e degradazione nel cristallo se non si adottano precauzioni come il raffreddamento.
Breve storia e contributi fondamentali
La cristallografia a raggi X fu sviluppata grazie al lavoro congiunto di Sir William Bragg (1862-1942) e di suo figlio Sir Lawrence Bragg (1890-1971). Per questi studi ricevettero il Premio Nobel per la Fisica per il 1915. Lawrence Bragg rimane la persona più giovane ad aver ottenuto un Nobel scientifico e, in seguito, fu direttore del Cavendish Laboratory della Cambridge University, dove lavorarono e si incontrarono figure chiave come James D. Watson e Francis Crick insieme a Maurice Wilkins e Rosalind Franklin nello studio che portò alla scoperta della struttura del DNA nel 1953.
Principio di base: diffrazione e legge di Bragg
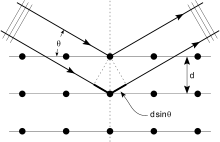
La tecnica fondamentale è la diffrazione a raggi X (XRD). In un esperimento di diffrazione un fascio di raggi X colpisce un cristallo e gli strati regolari di atomi fanno sì che i raggi diffratti diano origine a un insieme di massimi e minimi di intensità. La condizione per l'interferenza costruttiva è descritta dalla legge di Bragg: nλ = 2d sin θ, dove λ è la lunghezza d'onda dei raggi X, d la distanza tra piani reticolari e θ l’angolo di incidenza. Misurando le posizioni e le intensità dei massimi di diffrazione si ricava la distribuzione degli atomi all'interno della unit cell del cristallo.
Preparazione del campione
- Per la cristallografia a raggi X su singolo cristallo è necessario ottenere cristalli di qualità sufficiente (dimensione, regolarità e bassa imperfezione).
- Nel caso di campioni polverizzati si usa la diffrazione di polveri (powder XRD), che fornisce informazioni su fasi, parametri reticolari e orientamento medio, ma con dettagli atomici spesso meno diretti rispetto al cristallo singolo.
- Per proteine e macromolecole biologiche sono comuni tecniche di cristallizzazione in goccioline e il raffreddamento a temperature criogeniche per ridurre i danni da radiazione.
Acquisizione dati ed elaborazione
Un apparato tipico comprende una sorgente di raggi X, un goniometro per orientare il cristallo e un rivelatore moderno (ad es. detector a pixel) che registra il pattern di diffrazione. I dati grezzi (posizioni e intensità dei picchi) vengono processati con software specifici per ottenere una mappa di densità elettronica. Un passaggio fondamentale è il cosiddetto problema delle fasi: dalle intensità dei picchi si ottengono solo i moduli delle ampiezze della trasformata di Fourier, ma non le fasi. Per risolvere le fasi si utilizzano metodi come la sostituzione isomorfa multipla (MIR), anomalous dispersion (SAD/MAD) o la sostituzione molecolare (molecular replacement) quando è disponibile una struttura simile.
Costruzione del modello e validazione
Dalla mappa di densità elettronica si costruisce un modello atomico che viene successivamente raffinato per minimizzare le differenze tra dati sperimentali e pattern calcolato. Gli indicatori di qualità più usati sono il R-factor e il R-free, oltre alla risoluzione espressa in Ångström (più è bassa la cifra, più dettagliata è la struttura). La validazione include controlli geometrici e di stereochimica per garantire che il modello sia coerente con la chimica nota.
Applicazioni
- Chimica e scienza dei materiali: determinazione di strutture cristalline, studio di difetti e proprietà elettroniche.
- Biologia strutturale: studio di proteine, acidi nucleici e complessi macromolecolari; fondamentale per la structure-based drug design.
- Mineralogia e geoscienze: identificazione di fasi minerali e misurazione di parametri reticolari.
- Industria farmaceutica: comprensione dei siti attivi e progettazione di inibitori.
Limiti e alternative
La cristallografia richiede cristalli di buona qualità per le analisi a singolo cristallo; per campioni che non cristallizzano esistono alternative come la microscopia elettronica a crio (cryo-EM) o la spettroscopia NMR per molecole in soluzione. Inoltre, l’irraggiamento può causare danni (radicali, rottura dei legami) specialmente in cristalli biologici; per questo si applicano strategie di minimizzazione del danno (raffreddamento, raccolta rapida di dati). La risoluzione raggiungibile dipende dalla qualità del cristallo e dalla potenza della sorgente: sorgenti di sincrotrone e detector avanzati hanno ampliato enormemente le capacità della tecnica.
Conclusione
La cristallografia a raggi X rimane una delle tecniche più potenti per conoscere la disposizione atomica nelle sostanze solide e nelle macromolecole. Grazie ai progressi sperimentali, ai metodi computazionali e alle sorgenti di raggi X di nuova generazione, oggi è possibile ottenere strutture con grande dettaglio e usare queste informazioni per scoperte in chimica, biologia e tecnologia dei materiali.