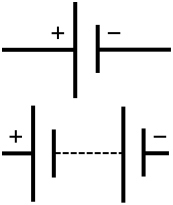Una batteria può essere composta da una
cella o da molte
celle. Ogni cella ha un anodo, un catodo e un elettrolita. L'elettrolita è il materiale principale all'interno della batteria. È spesso un tipo di acido e può essere pericoloso da toccare. L'anodo reagisce con l'elettrolita per produrre
elettroni (questa è l'estremità
negativa o
-). Il catodo reagisce con l'elettrolita e prende elettroni (questa è l'estremità
positiva o
+). Una
corrente elettrica avviene quando un filo collega l'anodo al catodo, e gli elettroni si muovono da un'estremità all'altra. (Ma una batteria può essere danneggiata solo da un filo che collega le due estremità, quindi è necessario anche un
carico tra le due estremità. Il carico è qualcosa che rallenta gli elettroni, e di solito fa qualcosa di utile, come una
lampadina in una
torcia, o l'
elettronica in una
calcolatrice).
L'elettrolita può essere liquido o solido. Una batteria è chiamata batteria a celle umide o a celle secche, a seconda del tipo di elettrolita.
Le reazioni chimiche che avvengono in una batteria sono reazioni esotermiche. Questo tipo di reazione produce calore. Per esempio, se lasci il tuo computer portatile acceso per molto tempo e poi tocchi la batteria, questa sarà calda o bollente.
Una batteria ricaricabile si ricarica invertendo la reazione chimica che avviene all'interno della batteria. Ma una batteria ricaricabile può essere ricaricata solo un certo numero di volte (durata di ricarica). Anche le batterie integrate non possono essere ricaricate per sempre. Inoltre, ogni volta che una batteria viene ricaricata, la sua capacità di mantenere la carica diminuisce un po'. Le batterie non ricaricabili non dovrebbero essere caricate perché possono fuoriuscire varie sostanze nocive, come l'idrossido di potassio.
Le celle possono essere collegate per fare una batteria più grande. Collegare il positivo di una cella al negativo della cella successiva si chiama collegarle in serie. La tensione di ogni batteria viene sommata. Due batterie da sei volt collegate in serie faranno 12 volt.
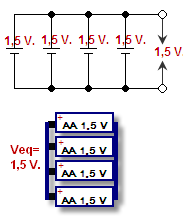
Collegare il positivo di una cella al positivo dell'altra e il negativo al negativo si chiama collegarle in parallelo. La tensione rimane la stessa, ma la corrente viene sommata. La tensione è la pressione che spinge gli elettroni attraverso i fili, si misura in volt. La corrente è la quantità di elettroni che possono passare contemporaneamente, si misura in ampere. La combinazione di corrente e tensione è la potenza (watt = volt x ampere) della batteria.