Ossigeno
L'ossigeno è l'elemento chimico con il simbolo O e il numero atomico 8. È il terzo elemento più comune nell'universo, dopo l'idrogeno e l'elio. Quando sono soli, due atomi di ossigeno di solito si legano per formare diossigeno (O2), un gas incolore. Non ha né sapore né odore. È di un azzurro pallido come liquido e solido. Il gas diossigeno costituisce il 20,8% dell'atmosfera terrestre. L'ossigeno fa parte del gruppo del calcogeno sulla tavola periodica e il suo numero atomico è 8. È un non metallo molto reattivo. Produce anche ossidi con molti elementi. Gli ossidi costituiscono quasi la metà della crosta terrestre.
La maggior parte della vita sulla Terra assorbe ossigeno gassoso (O2) da utilizzare per la respirazione. Molte molecole organiche negli esseri viventi hanno ossigeno in loro, come proteine, acidi nucleici, carboidrati e grassi. L'ossigeno è una parte dell'acqua, di cui tutta la vita conosciuta ha bisogno per vivere. Le piante producono la diossina della Terra attraverso la fotosintesi, utilizzando la luce del Sole per separare l'ossigeno dall'acqua e dall'anidride carbonica. L'ozono (O3) si trova nella parte superiore dell'atmosfera terrestre nello strato di ozono. Esso assorbe le radiazioni ultraviolette, che riducono le radiazioni che raggiungono il livello del suolo.
L'ossigeno fu isolato da Michael Sendivogius prima del 1604. Si pensa spesso che l'elemento sia stato scoperto da Carl Wilhelm Scheele, in Svezia, nel 1773, o da JosephPriestley, in Inghilterra, nel 1774. Priestly è di solito ritenuto il principale scopritore perché la sua opera è stata pubblicata per prima, anche se lui la chiamava "aria sofisticata", e non pensava che si trattasse di un elemento chimico. Antoine Lavoisier inventò il nome di ossigeno nel 1777 e fu il primo a dire che si trattava di un elemento chimico. Aveva anche ragione sul modo in cui aiuta il funzionamento della combustione.
L'ossigeno viene utilizzato per la produzione di acciaio, plastica, tessuti, propellente per razzi e per la saldatura.
Storia
I primi esperimenti
Uno dei primi esperimenti conosciuti su come la combustione ha bisogno di aria è stato effettuato dal greco Filone di Bisanzio nel II secolo a.C.. Egli scrisse nella sua opera Pneumatica che capovolgendo un vaso su una candela accesa e mettendo dell'acqua intorno a questo vaso, una parte dell'acqua entrava nel vaso. Filone pensava che ciò fosse dovuto al fatto che l'aria era stata trasformata nell'elemento classico del fuoco. Questo era sbagliato. Molto tempo dopo, Leonardo da Vinci ha correttamente calcolato che l'aria si esaurisce quando avviene la combustione, che costringe l'acqua a entrare nel recipiente.
Alla fine del XVII secolo, Robert Boyle scoprì che l'aria è necessaria per la combustione. Il chimico inglese John Mayow aggiunse a questo, mostrando che il fuoco aveva bisogno solo di una parte di aria. Ora lo chiamiamo ossigeno (sotto forma di di diossigeno). In uno dei suoi esperimenti, egli scoprì che mettendo una candela in un contenitore chiuso, l'acqua faceva salire l'acqua per sostituire un quattordicesimo del volume dell'aria nel contenitore, prima di spegnersi. La stessa cosa accadde quando un topo fu messo nel contenitore. Da questo, ha capito che l'ossigeno viene usato per la respirazione e la combustione.
Teoria dei flogisti
Robert Hooke, Ole Borch, Mikhail Lomonosov e Pierre Bayen hanno tutti fatto l'ossigeno negli esperimenti del XVII e XVIII secolo. Nessuno di loro pensava che fosse un elemento chimico. Ciò fu probabilmente dovuto all'idea della teoria del flogisto. Questo era ciò che la maggior parte delle persone credeva causasse combustione e corrosione.
J. J. Becher lo ideò nell'anno 1667, e Georg Ernst Stahl vi aggiunse nel 1731. La teoria del flogisto affermava che tutti i materiali combustibili erano composti da due parti. Una parte, chiamata flogisto, veniva rilasciata quando la sostanza che la conteneva veniva bruciata.
Si pensava che i materiali molto combustibili che lasciano solo una piccola quantità di residui, come il legno o il carbone, fossero fatti di flogisto. Le cose che si corrodono, come il ferro, si pensava contenessero solo una piccola quantità. L'aria non faceva parte di questa teoria.
Scoperta
L'alchimista, filosofo e medico polacco Michael Sendivogius ha parlato di una sostanza nell'aria, chiamandola "cibo della vita". Sendivogius ha scoperto, tra il 1598 e il 1604, che la sostanza è la stessa che si produce durante la decomposizione termica del nitrato di potassio. Alcuni credono che questa sia stata la scoperta dell'ossigeno, mentre altri non sono d'accordo.
Si dice spesso anche che l'ossigeno sia stato scoperto per la prima volta dal farmacista svedese Carl Wilhelm Scheele. Egli creò l'ossigeno riscaldando l'ossido di mercurio e alcuni nitrati nel 1771. Scheele chiamava il gas che produceva "aria di fuoco", perché era l'unico gas conosciuto che permetteva la combustione. Pubblicò la sua scoperta nel 1777.
Il 1° agosto 1774, un esperimento condotto dal sacerdote britannico Joseph Priestley concentrò la luce del sole sull'ossido di mercurio in un tubo di vetro. Questo fece un gas che lui chiamò "aria sofisticata". Scoprì anche che le candele bruciavano più intensamente nel gas e i topi vivevano più a lungo respirandolo. Quando respirava il gas, diceva (semplificato) "Sembrava aria normale, ma i miei polmoni si sentivano più leggeri e facili dopo". Le sue scoperte furono pubblicate nel 1775. Poiché le sue scoperte furono pubblicate per prime, di solito si dice che sia lo scopritore dell'ossigeno.
Il chimico francese Antoine Lavoisier disse più tardi di aver scoperto la sostanza. Il sacerdote gli fece visita nel 1774 e gli raccontò del suo esperimento. Scheele inviò anche una lettera a Lavoisier in quell'anno che parlava della sua scoperta.
Il contributo di Lavoisier
Lavoisier ha effettuato i primi esperimenti principali sull'ossidazione e ha dato la prima giusta spiegazione su come funziona la combustione. Ha usato questi ed altri esperimenti per dimostrare che la teoria del flogisto era sbagliata. Ha anche cercato di dimostrare che la sostanza scoperta da Priestley e Scheele era un elemento chimico.
In un esperimento, Lavoisier ha scoperto che non c'è stato alcun aumento di massa quando lo stagno e l'aria sono stati riscaldati in un contenitore chiuso. Ha anche scoperto che l'aria entrava in fretta quando il contenitore veniva aperto. Dopo di ciò, trovò che lo stagno era aumentato di massa della stessa quantità di quella dell'aria che entrava in fretta. Pubblicò le sue scoperte nel 1777. Scrisse che l'aria era composta da due gas. Uno lo chiamò "aria vitale" (ossigeno), necessario per la combustione e la respirazione. L'altro chiamò "azote" (azoto), che in greco significa "senza vita". Questo è ancora il nome dell'azoto in alcune lingue, compreso il francese.
Lavoisier ha rinominato "aria vitale" in "oxygène", che in greco significa "produttore di acidi". Lo chiamò così perché pensava che l'ossigeno fosse in tutti gli acidi, il che era sbagliato. Molti chimici si resero conto che Lavoiser aveva sbagliato il nome, ma il nome era ormai troppo comune per poterlo cambiare.
"Oxygen" divenne il nome in lingua inglese, anche se gli scienziati inglesi erano contrari.
Storia successiva
La teoria degli atomi di John Dalton diceva che tutti gli elementi avevano un solo atomo e che gli atomi nei composti erano di solito soli. Per esempio, egli pensava erroneamente che l'acqua (H2O) avesse la formula del solo HO. Nel 1805, Joseph Louis Gay-Lussac e Alexander von Humboldt dimostrarono che l'acqua è composta da due atomi di idrogeno e un atomo di ossigeno. Nel 1811, Amedeo Avogadro capì correttamente di cosa era fatta l'acqua in base alla legge di Avogadro.
Alla fine del XIX secolo, gli scienziati scoprirono che l'aria poteva essere trasformata in un liquido e che i composti in essa contenuti potevano essere isolati comprimendo e raffreddando l'aria. Il chimico e fisico svizzero Raoul Pictet scoprì l'ossigeno liquido facendo evaporare l'anidride solforosa per trasformare l'anidride carbonica in un liquido. Questo è stato poi anche evaporato per raffreddare il gas di ossigeno per trasformarlo in un liquido. Il 22 dicembre 1877 inviò un telegramma all'Accademia francese delle scienze per informarli della sua scoperta.

Lavoisier all'Accademia-Louis Ernest Barrias
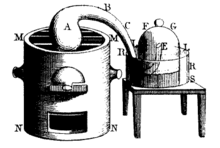
Aria di decomposizione Lavoisier
Caratteristiche
Proprietà e struttura molecolare
A temperatura e pressione standard, l'ossigeno non ha colore, odore o sapore ed è un gas con la formula chimica O
2 chiamato diossigeno.
Come diossigeno, due atomi di ossigeno sono chimicamente legati l'uno all'altro. Questo legame può essere chiamato molte cose, ma semplicemente chiamato un doppio legame covalente. La diossigeno è molto reattivo e può reagire con molti altri elementi. Gli ossidi si formano quando gli elementi metallici reagiscono con la diossigeno, come l'ossido di ferro, noto come ruggine. Ci sono molti composti di ossido sulla Terra.
Allotropi
L'allotropio comune (tipo) di ossigeno sulla Terra è chiamato diossigeno (O2). Questa è la seconda parte più grande dell'atmosfera terrestre, dopo l'azoto (N2). L'O2 ha una lunghezza di legame di 121 pm e un'energia di legame di 498 kJ/mol A causa della sua energia, l'O2 è usato dalla vita complessa come gli animali.
L'ozono (O3) è molto reattivo e danneggia i polmoni quando viene respirato. L'ozono è prodotto nell'alta atmosfera quando l'O2 si combina con l'ossigeno puro prodotto quando l'O2 è diviso dalle radiazioni ultraviolette. L'ozono assorbe molte radiazioni nella parte UV dello spettro elettromagnetico e quindi lo strato di ozono nell'alta atmosfera protegge la Terra dalle radiazioni.
Il tetraossigeno (O4) è stato scoperto nel 2001. Esiste solo in condizioni estreme quando si esercita una forte pressione sull'O2.
Proprietà fisiche
L'ossigeno si dissolve più facilmente dall'aria nell'acqua rispetto all'azoto. Quando c'è la stessa quantità di aria e acqua, c'è una molecola di O2 ogni 2 molecole di N2 (un rapporto di 1:2). Questo è diverso dall'aria, dove c'è un rapporto 1:4 tra ossigeno e azoto. È anche più facile per l'O2 sciogliersi in acqua dolce che in acqua di mare. L'ossigeno si condensa a 90,20 K (-182,95 °C, -297,31 °F) e si congela a 54,36 K (-218,79 °C, -361,82 °F). Sia l'O2 liquido che quello solido sono trasparenti e di colore azzurro.
L'ossigeno è molto reattivo e deve essere tenuto lontano da tutto ciò che può bruciare.
Isotopi
In natura ci sono tre isotopi stabili di ossigeno. Sono 16O, 17O e 18O. Circa il 99,7% dell'ossigeno è l'isotopo 16O.
Evento
| I dieci elementi più comuni nella galassia della Via Lattea sono stati stimati spettroscopicamente | ||||
| Z | Elemento | Frazione di massa in parti per milione | ||
| 1 | 739,000 | 71 × massa di ossigeno (barra rossa) | ||
| 2 | 240,000 | 23 × massa di ossigeno (barra rossa) | ||
| 8 | Ossigeno | 10,400 | 10400
| |
| 6 | 4,600 | 4600
| ||
| 10 | Neon | 1,340 | 1340
| |
L'ossigeno è l'elemento più comune per massa sulla Terra. È il terzo elemento più comune nell'universo, dopo l'idrogeno e l'elio. Circa lo 0,9% della massa del Sole è ossigeno. L'ossigeno costituisce il 49,2% della crosta terrestre in massa come parte di composti di ossido come il biossido di silicio. È anche la parte principale degli oceani della Terra, costituendo l'88,8% della massa. Il gas ossigeno è la seconda parte più comune dell'atmosfera, costituendo il 20,8% della sua massa e il 23,1% del suo volume. La Terra è strana rispetto ad altri pianeti conosciuti, in quanto una grande quantità della sua atmosfera è costituita da ossigeno gassoso. Marte ha lo 0,1% di O2 in volume, mentre il resto del pianeta del Sistema Solare ne ha meno.
L'elevata quantità di ossigeno gassoso sulla Terra è dovuta al ciclo dell'ossigeno. Questo è controllato principalmente dalla fotosintesi, che rende l'ossigeno gassoso dall'anidride carbonica, dall'acqua e dall'energia del Sole. La respirazione porta poi il gas di ossigeno fuori dall'atmosfera e lo ritrasforma in anidride carbonica e acqua. Questo avviene alla stessa velocità, quindi la quantità di ossigeno gassoso e di anidride carbonica non cambia a causa di essa.
Utilizza
Medico
L'O2 è una parte molto importante della respirazione. Per questo motivo, è usato in medicina. Viene utilizzato per aumentare la quantità di ossigeno nel sangue di una persona in modo che possa avvenire una maggiore respirazione. Questo può farli diventare più sani più velocemente se sono malati. L'ossigenoterapia è usata per trattare l'enfisema, la polmonite, alcuni problemi cardiaci, e qualsiasi malattia che rende più difficile per una persona a prendere l'ossigeno.
Supporto vitale
L'O2 a bassa pressione viene utilizzato nelle tute spaziali, circondando il corpo con il gas. Si usa ossigeno puro, ma ad una pressione molto più bassa. Se la pressione fosse più alta, sarebbe velenoso.

Un concentratore di ossigeno in casa di un paziente con enfisema
Sicurezza
L'NFPA 704 di Oxygen's dice che il gas di ossigeno compresso non è pericoloso per la salute e non è infiammabile.
Tossicità
Ad alte pressioni, il gas ossigeno (O2) può essere pericoloso per gli animali, compresi gli esseri umani. Può causare convulsioni e altri problemi di salute. La tossicità dell'ossigeno di solito inizia a verificarsi a pressioni superiori a 50 kilopascal (kPa), pari a circa il 50% di ossigeno nell'aria a pressione standard (l'aria sulla Terra ha circa il 20% di ossigeno).
I neonati prematuri venivano messi in scatole con aria con un'elevata quantità di O2. Questo è stato fermato quando alcuni bambini sono diventati ciechi a causa dell'ossigeno.
La respirazione di O2 puro nelle tute spaziali non provoca alcun danno perché viene utilizzata una pressione inferiore.
Combustione e altri pericoli
Quantità concentrate di O2 puro possono causare un rapido incendio. Quando l'ossigeno concentrato e i combustibili vengono avvicinati tra loro, una leggera accensione può causare un enorme incendio. L'equipaggio dell'Apollo 1 è stato ucciso da un incendio a causa dell'ossigeno concentrato utilizzato nell'aria della capsula.
Se l'ossigeno liquido viene versato su composti organici, come il legno, può esplodere.
Domande e risposte
D: Qual è il simbolo dell'ossigeno?
R: Il simbolo dell'ossigeno è O.
D: Quanti atomi di ossigeno si trovano solitamente nel diossigeno (O2)?
R: Il diossigeno (O2) contiene in genere due atomi di ossigeno.
D: Di che colore è l'ossigeno liquido o solido?
R: L'ossigeno liquido o solido è di colore blu pallido.
D: A quale gruppo della tavola periodica appartiene l'ossigeno?
R: L'ossigeno appartiene al gruppo dei calcogeni della tavola periodica.
D: Quanto volume dell'atmosfera terrestre è costituito da ossigeno?
R: L'ossigeno costituisce più di un quinto dell'atmosfera terrestre in volume.
D: In che modo le piante e gli altri organismi producono la maggior parte dell'ossigeno atmosferico della Terra?
R: Le piante e gli altri organismi producono la maggior parte dell'ossigeno atmosferico della Terra attraverso la fotosintesi, che prevede l'utilizzo della luce solare per convertire l'acqua in idrogeno e rilasciare ossigeno come sottoprodotto.
D: Quali usi ha la forma liquida o solidificata dell'ossigeno?
R: Le forme liquide o solidificate di ossigeno possono essere utilizzate come propellenti per i razzi, per la saldatura, per scopi medici e per respirare quando non è disponibile aria buona (ad esempio, per i sommozzatori e i vigili del fuoco).
Cerca nell'enciclopedia