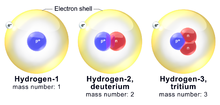
Gli atomi di un elemento chimico possono esistere in diversi tipi. Questi sono chiamati isotopi. Hanno lo stesso numero di protoni (ed elettroni), ma un numero diverso di neutroni. I diversi isotopi dello stesso elemento hanno masse diverse. Massa è la parola che indica quanta sostanza (o materia) ha qualcosa. Le cose con masse diverse hanno pesi diversi. Poiché isotopi diversi hanno un numero diverso di neutroni, non tutti hanno lo stesso peso o la stessa massa.
I diversi isotopi dello stesso elemento hanno lo stesso numero atomico. Hanno lo stesso numero di protoni. Il numero atomico è deciso dal numero di protoni. Gli isotopi hanno però numeri di massa diversi, perché hanno numeri di neutroni diversi.
La parola isotopo, che significa nello stesso punto, deriva dal fatto che gli isotopi si trovano nello stesso punto della tavola periodica.
In un atomo neutro, il numero di elettroni è uguale al numero di protoni. Anche gli isotopi dello stesso elemento hanno lo stesso numero di elettroni e la struttura elettronica. Poiché il modo in cui un atomo agisce è deciso dalla sua struttura elettronica, gli isotopi sono quasi gli stessi chimicamente, ma diversi fisicamente dai loro atomi originali.
Gli isotopi più pesanti reagiscono chimicamente più lentamente degli isotopi più leggeri dello stesso elemento. Questo "effetto massa" è più grande per il prozio (1H) e il deuterio (2H), perché il deuterio ha una massa doppia rispetto al prozio. Per gli elementi più pesanti, il rapporto di peso atomico relativo tra gli isotopi è molto inferiore, e l'effetto massa è di solito piccolo.