La tavola periodica degli elementi chimici è una rappresentazione ordinata di tutti gli elementi chimici noti. Nella tabella gli elementi sono disposti secondo il loro numero atomico, che aumenta da sinistra a destra e dall'alto in basso, a partire dal più piccolo, l'idrogeno. Il numero atomico di un elemento corrisponde al numero di protoni presenti nel nucleo di un atomo. La disposizione regolare degli elementi nella tavola riflette la periodicità delle loro proprietà chimiche e fisiche, nota come legge periodica; grazie a questa struttura è possibile confrontare e prevedere il comportamento degli elementi.
Struttura della tavola periodica
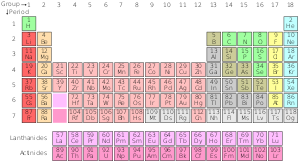
Gli elementi sono organizzati in periodi e gruppi. Una fila orizzontale è chiamata periodo e ogni periodo ha un numero (da 1 a 7/8 a seconda della rappresentazione). I periodi indicano il livello di energia principale degli elettroni; gli elementi in uno stesso periodo hanno numeri atomici consecutivi. Il primo periodo contiene solo 2 elementi: idrogeno ed elio. I periodi 2 e 3 contengono ciascuno 8 elementi, mentre i periodi successivi sono più lunghi perché coinvolgono il riempimento di sottolivelli diversi (s, p, d, f).
Una colonna verticale è chiamata gruppo. Nella tavola periodica standard ci sono 18 gruppi numerati da 1 a 18 secondo il sistema adottato dall'Unione Internazionale di Chimica Pura e Applicata (IUPAC). Gli elementi dello stesso gruppo hanno configurazioni elettroniche esterne simili, cioè lo stesso numero di elettroni di valenza, e per questo mostrano proprietà chimiche simili. Ad esempio, il gruppo 18 è noto come gas nobile perché i suoi membri sono gas poco reattivi e tendono a non combinarsi con altri atomi.
Per chiarezza di lettura la tavola viene spesso suddivisa in blocchi elettronici:
- Blocco s (gruppi 1–2): elementi con elettroni esterni nel sottolivello s;
- Blocco p (gruppi 13–18): contiene i non metalli e molti metalloidi;
- Blocco d (gruppi 3–12): corrisponde ai metalli di transizione;
- Blocco f: comprende i lantanidi e gli attinidi (generalmente mostrati come due file separate sotto la tabella principale) e deriva dal riempimento degli orbitali f.
Classificazione degli elementi
Gli elementi della tavola periodica si possono raggruppare in tre categorie principali: metalli, metalloidi e non metalli. In generale:
- I metalli (in basso a sinistra della tavola) sono di solito lucenti, malleabili, duttili e buoni conduttori di calore ed elettricità (ad esempio il cesio è molto metallico rispetto a elementi come l'elio).
- I non metalli (in alto a destra) comprendono gas, liquidi e solidi fragili, con scarsa conducibilità elettrica.
- I metalloidi hanno proprietà intermedie tra metalli e non metalli e spesso mostrano comportamento semiconduttore.
Altre famiglie importanti nella tavola periodica:
- Alcalini (gruppo 1, molto reattivi con l'acqua)
- Alcalino-terrosi (gruppo 2)
- Alogeni (gruppo 17, non metalli fortemente reattivi)
- Metalli di transizione (blocchi d)
- Lantanidi e attinidi (serie f, spesso poste separatamente)
Tendenze periodiche
La tavola consente di osservare diverse tendenze regolari quando si muove attraverso periodi o gruppi:
- Raggio atomico: aumenta scendendo un gruppo e diminuisce procedendo lungo un periodo da sinistra a destra.
- Energia di ionizzazione: l'energia necessaria per rimuovere un elettrone; generalmente diminuisce scendendo un gruppo e aumenta lungo un periodo verso destra.
- Elettronegatività: tendenza di un atomo ad attrarre elettroni in un legame chimico; aumenta lungo un periodo verso destra e diminuisce scendendo un gruppo.
- Affinità elettronica: varia con il posizionamento nella tavola ed è correlata alla facilità con cui un atomo accetta un elettrone.
Storia e sviluppo
La tavola periodica moderna ha origine dagli studi di diversi scienziati, ma fu il chimico russo Dmitry Ivanovich Mendeleyev (1834–1907) a formulare, nel 1869, una versione che ordinava gli elementi per proprietà chimiche e lasciava spazi vuoti per elementi ancora da scoprire. La capacità di Mendeleyev di predire le proprietà di elementi ignoti rese la sua versione particolarmente influente. In suo onore è stato denominato l'elemento 101, il mendelevio.
Nel corso del XX e XXI secolo la tavola è stata aggiornata man mano che venivano scoperti o sintetizzati nuovi elementi. Attualmente l'IUPAC riconosce 118 elementi chimici confermati e assegna loro nomi e simboli ufficiali. L'IUPAC ha anche stabilito il sistema di numerazione dei gruppi in numeri arabi (1–18) per un uso uniforme a livello internazionale; in passato si utilizzavano sistemi con numeri romani o notazioni miste.
Elementi sintetici, isotopi e stabilità
Molti elementi con numero atomico elevato sono stati prodotti artificialmente in laboratorio mediante reazioni nucleari. Questi elementi sintetici spesso hanno isotopi molto instabili con emivite molto brevi; alcuni decadono in poche frazioni di secondo, altri possono persistere più a lungo. La chimica e la fisica di questi elementi sono oggetto di ricerche avanzate per comprendere la struttura nucleare e i limiti della materia ordinaria.
Uso e importanza
La tavola periodica è uno strumento fondamentale per i chimici, i fisici, gli ingegneri e gli studenti. Serve a:
- predire il tipo di legami e le reattività degli elementi;
- organizzare i materiali in base alle proprietà fisiche e chimiche;
- fornire un quadro di riferimento per ricerche e applicazioni tecnologiche (materiali, catalisi, semiconduttori, medicina, ecc.).
In sintesi, la tavola periodica è più di un semplice elenco: è una mappa delle proprietà atomiche che mette in relazione struttura elettronica e comportamento chimico, rendendo possibile la previsione e la scoperta scientifica.