Il calore può indurre i doppi legami a formare un anello. Le cicloaddizioni termiche di solito hanno (4n + 2) elettroni π che partecipano al materiale di partenza, per qualche numero intero n. A causa della simmetria orbitale, la maggior parte delle cicloaddizioni sono suprafacciali-suprafacciali. Raramente, sono antarafacciali-antarafacciali. Ci sono alcuni esempi di cicliedizioni termiche che hanno 4n elettroni π (per esempio la [2 + 2] cicloaddizione). Queste procedono in senso soprafacciale-antarafacciale. Per esempio, la dimerizzazione del chetene ha un insieme ortogonale di orbitali p. Questi orbitali p permettono alla reazione di procedere utilizzando uno stato di transizione incrociato.
La luce può anche indurre i doppi legami a formare un anello. Le cicloaddizioni in cui partecipano 4n elettroni π possono anche verificarsi come risultato dell'attivazione fotochimica. Qui, un componente fa muovere un elettrone dal più alto orbitale molecolare occupato (HOMO) (π bonding) al più basso orbitale molecolare non occupato (LUMO) (π* antibonding). Dopo che l'elettrone è promosso all'orbitale più alto, la simmetria orbitale permette alla reazione di procedere in modo suprafacciale-suprafacciale. Un esempio è la reazione di DeMayo. Un altro esempio è mostrato qui sotto, la dimerizzazione fotochimica dell'acido cinnamico.
Si noti che non tutte le ciclizzazioni fotochimiche (2+2) sono cycloadditions; alcune sono note per operare con meccanismi radicali.
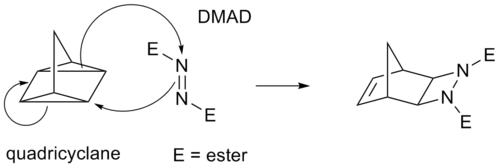
Alcune cicloaddizioni invece di legami π operano attraverso anelli ciclopropanici tesi; poiché questi hanno un carattere π significativo. Per esempio, un analogo della reazione Diels-Alder è la reazione quadriciclano-DMAD:
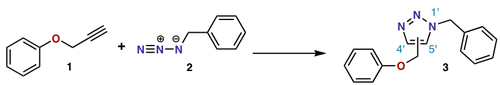
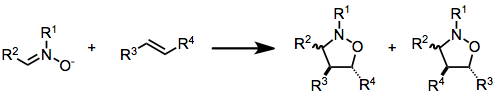
Nella notazione di cicloaddizione (i+j+...) i e j si riferiscono al numero di atomi coinvolti nella cicloaddizione. In questa notazione una reazione di Diels-Alder è una (4+2) cicloaddizione e un'addizione 1,3-dipolare come il primo passo dell'ozonolisi è una (3+2) cocloaddizione. Questa notazione usa le parentesi. La notazione IUPAC preferita, tuttavia, con [i+j+...] conta gli elettroni e non gli atomi. Utilizza le parentesi quadre. In questa notazione, la reazione Diels-Alder e la reazione dipolare diventano entrambe una [4+2]cicloaddizione. La reazione tra norbornadiene e un alchene attivato è una [2+2+2]cicloaddizione.
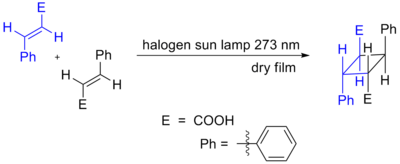
.png)
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)