Due definizioni
La tensione superficiale, rappresentata dal simbolo γ è definita come la forza lungo una linea di lunghezza unitaria, dove la forza è parallela alla superficie ma perpendicolare alla linea. Un modo per immaginare questo è quello di immaginare una pellicola di sapone piatta delimitata su un lato da un filo teso di lunghezza L. Il filo sarà tirato verso l'interno della pellicola da una forza pari a 2 γ {displaystyle \scriptstyle \gamma }  L (il fattore 2 è perché la pellicola di sapone ha due lati, quindi due superfici). La tensione superficiale si misura quindi in forze per unità di lunghezza. La sua unità SI è newton per metro, ma si usa anche l'unità cgs di dyne per cm. Un dyn/cm corrisponde a 0,001 N/m.
L (il fattore 2 è perché la pellicola di sapone ha due lati, quindi due superfici). La tensione superficiale si misura quindi in forze per unità di lunghezza. La sua unità SI è newton per metro, ma si usa anche l'unità cgs di dyne per cm. Un dyn/cm corrisponde a 0,001 N/m.
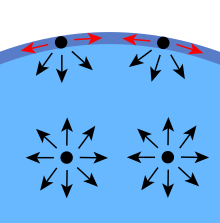
Una definizione equivalente, utile in termodinamica, è il lavoro fatto per unità di superficie. Come tale, per aumentare la superficie di una massa di liquido di una quantità, δA, una quantità di lavoro, γ {displaystyle \scriptstyle \gamma }  δA, è necessaria. Questo lavoro è immagazzinato come energia potenziale. Di conseguenza la tensione superficiale può essere misurata anche nel sistema SI come joule per metro quadrato e nel sistema cgs come ergs per cm2. Poiché i sistemi meccanici cercano di trovare uno stato di minima energia potenziale, una goccia libera di liquido assume naturalmente una forma sferica, che ha la minima area superficiale per un dato volume.
δA, è necessaria. Questo lavoro è immagazzinato come energia potenziale. Di conseguenza la tensione superficiale può essere misurata anche nel sistema SI come joule per metro quadrato e nel sistema cgs come ergs per cm2. Poiché i sistemi meccanici cercano di trovare uno stato di minima energia potenziale, una goccia libera di liquido assume naturalmente una forma sferica, che ha la minima area superficiale per un dato volume.
L'equivalenza della misura dell'energia per unità di superficie con la forza per unità di lunghezza può essere dimostrata dall'analisi dimensionale.
Curvatura della superficie e pressione
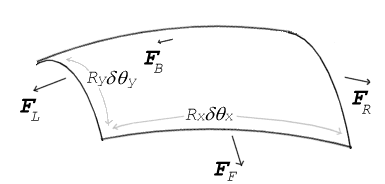
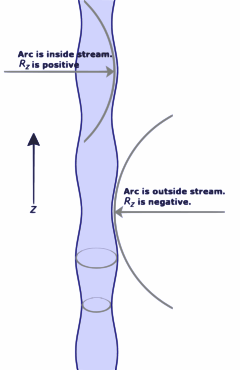
Se nessuna forza agisce normalmente a una superficie in tensione, la superficie deve rimanere piatta. Ma se la pressione su un lato della superficie differisce dalla pressione sull'altro lato, la differenza di pressione per l'area della superficie risulta in una forza normale. Affinché le forze di tensione superficiale annullino la forza dovuta alla pressione, la superficie deve essere curva. Il diagramma mostra come la curvatura di una piccola zona di superficie porta ad una componente netta delle forze di tensione superficiale che agiscono normalmente al centro della zona. Quando tutte le forze sono bilanciate, l'equazione risultante è nota come equazione di Young-Laplace:
Δ p = γ ( 1 R x + 1 R y ) {displaystyle \Delta p\ = \gamma \sinistra({frac {1}{R_{x}}+{frac {1}{R_{y}}} destra)} 
dove:
· Δp è la differenza di pressione.
· γ {displaystyle \scriptstyle \gamma }  è la tensione superficiale.
è la tensione superficiale.
· Rx e Ry sono i raggi di curvatura in ciascuno degli assi paralleli alla superficie.
La quantità tra parentesi sul lato destro è infatti (due volte) la curvatura media della superficie (a seconda della normalizzazione).
Le soluzioni di questa equazione determinano la forma delle gocce d'acqua, delle pozzanghere, dei menischi, delle bolle di sapone e di tutte le altre forme determinate dalla tensione superficiale. (Un altro esempio è la forma delle impronte che i piedi di uno strider d'acqua fanno sulla superficie di uno stagno).
La tabella qui sotto mostra come la pressione interna di una goccia d'acqua aumenta con il diminuire del raggio. Per gocce non molto piccole l'effetto è sottile, ma la differenza di pressione diventa enorme quando le dimensioni della goccia si avvicinano alla dimensione molecolare. (Nel limite di una singola molecola il concetto diventa privo di significato).
| Δp per gocce d'acqua di diverso raggio a STP |
| Raggio della goccia | 1 mm | 0,1 mm | 1 μm | 10 nm |
| Δp (atm) | 0.0014 | 0.0144 | 1.436 | 143.6 |
Superficie liquida
È difficile trovare la forma della superficie minima delimitata da una cornice di forma arbitraria usando solo la matematica. Eppure, costruendo il telaio con del filo di ferro e immergendolo nella soluzione di sapone, una superficie localmente minima apparirà nella pellicola di sapone risultante in pochi secondi.
La ragione di ciò è che la differenza di pressione attraverso un'interfaccia fluida è proporzionale alla curvatura media, come visto nell'equazione di Young-Laplace. Per un film di sapone aperto, la differenza di pressione è zero, quindi la curvatura media è zero, e le superfici minime hanno la proprietà della curvatura media zero.
Angoli di contatto
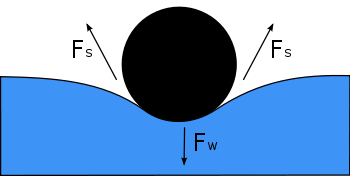
La superficie di qualsiasi liquido è un'interfaccia tra quel liquido e qualche altro mezzo. La superficie superiore di uno stagno, per esempio, è un'interfaccia tra l'acqua dello stagno e l'aria. La tensione superficiale, quindi, non è una proprietà del solo liquido, ma una proprietà dell'interfaccia del liquido con un altro mezzo. Se un liquido è in un contenitore, oltre all'interfaccia liquido/aria sulla sua superficie superiore, c'è anche un'interfaccia tra il liquido e le pareti del contenitore. La tensione superficiale tra il liquido e l'aria è solitamente diversa (maggiore) della sua tensione superficiale con le pareti di un contenitore. Dove le due superfici si incontrano, la geometria bilancerà tutte le forze.
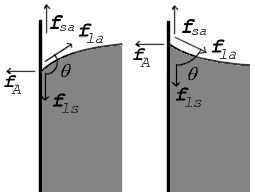
Dove le due superfici si incontrano, formano un angolo di contatto, θ {displaystyle \scriptstyle \theta }  che è l'angolo che la tangente alla superficie fa con la superficie solida. Il diagramma a destra mostra due esempi. Le forze di tensione sono mostrate per l'interfaccia liquido-aria, l'interfaccia liquido-solido e l'interfaccia solido-aria. L'esempio a sinistra è dove la differenza tra la tensione superficiale liquido-solido e solido-aria, γ l s - γ s a {displaystyle \scriptstyle \gamma _{mathrm {ls} \gamma _\mathrm {\mathrm {sa} }}
che è l'angolo che la tangente alla superficie fa con la superficie solida. Il diagramma a destra mostra due esempi. Le forze di tensione sono mostrate per l'interfaccia liquido-aria, l'interfaccia liquido-solido e l'interfaccia solido-aria. L'esempio a sinistra è dove la differenza tra la tensione superficiale liquido-solido e solido-aria, γ l s - γ s a {displaystyle \scriptstyle \gamma _{mathrm {ls} \gamma _\mathrm {\mathrm {sa} }}  è minore della tensione superficiale liquido-aria, γ l a {displaystyle \scriptstyle \gamma _{mathrm {la} }}
è minore della tensione superficiale liquido-aria, γ l a {displaystyle \scriptstyle \gamma _{mathrm {la} }}  ma è ancora positiva, cioè
ma è ancora positiva, cioè
γ l a > γ l s - γ s a > 0 {displaystyle \gamma _{mathrm {la} \gamma _\mathrm {\mathrm {ls} \gamma _\mathrm {\mathrm}- \mathrm {sa} }\ >\ 0} 
Nel diagramma, sia la forza verticale che quella orizzontale devono annullarsi esattamente nel punto di contatto, noto come equilibrio. La componente orizzontale di f l a {displaystyle \scriptstyle f_{mathrm {la}  è annullata dalla forza adesiva, f A {displaystyle \scriptstyle f_{mathrm {A} }}
è annullata dalla forza adesiva, f A {displaystyle \scriptstyle f_{mathrm {A} }}  .
.
f A = f l a sin θ {displaystyle f_{mathrm {A} == f_{mathrm {la} sin \theta } 
L'equilibrio di forze più importante, però, è nella direzione verticale. La componente verticale di f l a {displaystyle \scriptstyle f_{mathrm {la}  deve esattamente annullare la forza, f l s {displaystyle \scriptstyle f_{mathrm {ls} }}
deve esattamente annullare la forza, f l s {displaystyle \scriptstyle f_{mathrm {ls} }}  .
.
f l s - f s a = - f l a cos θ {displaystyle f_{mathrm {ls} f_{mathrm {sa} == -f_{mathrm {la} {\an8}Cos'è il cos'è il cos'è il cos'è il cos'è il cos'è il cos'è} 
| Liquido | Solido | Angolo di contatto |
| acqua | | vetro soda-lime | | vetro al piombo | | quarzo fuso | | 0° |
| etanolo |
| etere dietilico |
| tetracloruro di carbonio |
| glicerolo |
| acido acetico |
| acqua | cera di paraffina | 107° |
| argento | 90° |
| ioduro di metile | vetro soda-lime | 29° |
| vetro al piombo | 30° |
| quarzo fuso | 33° |
| mercurio | vetro soda-lime | 140° |
| Alcuni angoli di contatto liquido-solido |
Poiché le forze sono direttamente proporzionali alle rispettive tensioni superficiali, abbiamo anche:
γ l s - γ s a = - γ l a cos θ {displaystyle \gamma _{mathrm {ls} \gamma _\mathrm {\mathrm}- \gamma {\mathrm {\mathrm {\mathrm} == -\gamma _{mathrm {\mathrm {la} \cos \theta } 
dove
· γ l s {displaystyle \scriptstyle \gamma _{mathrm {ls}  è la tensione superficiale liquido-solido,
è la tensione superficiale liquido-solido,
· γ l a {displaystyle \scriptstyle \gamma _{mathrm {la}  è la tensione superficiale liquido-aria,
è la tensione superficiale liquido-aria,
· γ s a {displaystyle \scriptstyle \gamma _{mathrm {sa}  è la tensione superficiale solido-aria,
è la tensione superficiale solido-aria,
· θ {displaystyle \scriptstyle \theta } è l'angolo di contatto, dove un menisco concavo ha un angolo di contatto inferiore a 90° e un menisco convesso ha un angolo di contatto superiore a 90°.
è l'angolo di contatto, dove un menisco concavo ha un angolo di contatto inferiore a 90° e un menisco convesso ha un angolo di contatto superiore a 90°.
Questo significa che anche se la differenza tra la tensione superficiale liquido-solido e solido-aria, γ l s - γ s a {displaystyle \scriptstyle \gamma _{mathrm {ls} \gamma _\mathrm {\mathrm {sa} }}  è difficile da misurare direttamente, può essere dedotta dalla tensione superficiale liquido-aria, γ l a {displaystyle \scriptstyle \gamma _{mathrm {la} }} ,
è difficile da misurare direttamente, può essere dedotta dalla tensione superficiale liquido-aria, γ l a {displaystyle \scriptstyle \gamma _{mathrm {la} }} ,  e l'angolo di contatto di equilibrio, θ {displaystyle \scriptstyle \theta }
e l'angolo di contatto di equilibrio, θ {displaystyle \scriptstyle \theta }  che è una funzione degli angoli di contatto che avanzano e si allontanano, facilmente misurabili (vedi articolo principale angolo di contatto).
che è una funzione degli angoli di contatto che avanzano e si allontanano, facilmente misurabili (vedi articolo principale angolo di contatto).
Questa stessa relazione esiste nel diagramma a destra. Ma in questo caso vediamo che poiché l'angolo di contatto è inferiore a 90°, la differenza di tensione superficiale liquido-solido/solido-aria deve essere negativa:
γ l a > 0 > γ l s - γ s a {displaystyle \gamma _{mathrm {la} 0 > 0 > \gamma _\mathrm {\mathrm {\mathrm {ls} \gamma _\mathrm {\mathrm {sa} }} 
Angoli di contatto speciali
Si osservi che nel caso speciale di un'interfaccia acqua-argento dove l'angolo di contatto è uguale a 90°, la differenza di tensione superficiale liquido-solido/solido-aria è esattamente zero.
Un altro caso speciale è quello in cui l'angolo di contatto è esattamente 180°. L'acqua con Teflon appositamente preparato si avvicina a questo valore. L'angolo di contatto di 180° si verifica quando la tensione superficiale liquido-solido è esattamente uguale alla tensione superficiale liquido-aria.
γ l a = γ l s - γ s a > 0 θ = 180 ∘ {displaystyle \gamma _{mathrm {la} = \gamma _{mathrm {s} \gamma _\mathrm {\mathrm {sa} 0\qquadro \theta \= 180^{\circuito} 















































.jpg)