Modello atomico di Thomson
Il modello del budino di prugna era un primo (ed errato) modello di atomo del XX secolo. Fu proposto da J.J. Thomson nel 1904, dopo la scoperta dell'elettrone, ma prima della scoperta del nucleo atomico. In quel periodo, gli scienziati sapevano che c'era una carica positiva nell'atomo che bilanciava le cariche negative degli elettroni, rendendo l'atomo neutro, ma non sapevano da dove veniva la carica positiva. Il modello di Thomson mostrava un atomo che aveva un mezzo, o spazio, carico positivamente, con elettroni carichi negativamente all'interno del mezzo. Poco dopo la sua proposta, il modello fu chiamato modello 'plum pudding' perché il mezzo positivo era come un budino, con elettroni, o prugne, all'interno.

Esempio del modello di Thomson
Sviluppo nel moderno modello atomico
Il modello di Rutherford
In pratica, nel 1909, non molto tempo dopo che il modello di Thomson fu proposto, Hans Geiger e Ernest Marsden fecero un esperimento con sottili fogli d'oro, per testare il modello di Thomson. Il loro professore, Ernest Rutherford, si aspettava che i risultati provassero che Thomson aveva ragione, ma i risultati furono estremamente diversi da quello che si aspettavano. Nel 1911, Rutherford scoprì che le cariche positive provengono da minuscole particelle chiamate protoni, e che i protoni erano in un piccolo centro chiamato nucleo, e che gli elettroni orbitavano intorno al nucleo.
Modello di Bohr
Il modello di Rutherford era abbastanza semplice, ma era sbagliato perché gli elettroni hanno carica e dovrebbero essere attratti dal nucleo con carica positiva. Nel 1913, Niels Bohr aggiunse i "livelli di energia" al modello atomico. Gli elettroni non cadono nel nucleo perché sono contenuti in livelli di energia, e per passare a livelli di energia più alti è necessaria energia extra, e per passare a livelli di energia più bassi è necessario un rilascio di energia. Non è possibile cambiare stato energetico senza cambiare l'energia dell'elettrone. Se un elettrone viene colpito da un fotone (una particella che trasporta radiazione elettromagnetica) guadagnerà energia extra e passerà ad un livello di energia superiore (cambia stato), poi tornerà giù ad un livello di energia inferiore, rilasciando l'energia contenuta. Questo nuovo modello fu chiamato modello Bohr o modello Rutherford-Bohr. Questo aggiunse un intero nuovo ramo della scienza: La fisica quantistica.
Modello quantistico
Nel 1926 Erwin Schrödinger utilizzò l'idea che gli elettroni agissero come un'onda, oltre che come una particella, questo è noto come dualità onda-particella. Questo aggiunse un livello completamente nuovo al modello atomico e alla fisica quantistica. Con una particella, puoi sapere dove si trova nello spazio se la osservi (guardi). Ma con un'onda, è dappertutto, quindi non si può definire dove si trova esattamente. Questo è noto come incertezza quantistica. Con un elettrone, si può solo conoscere la probabilità che si trovi in un posto, perché è un'onda oltre che una particella. (Vedere il diagramma sopra)
Un'immagine che mostra un elettrone che cambia livello energetico e che guadagna e rilascia energia sotto forma di fotoni.
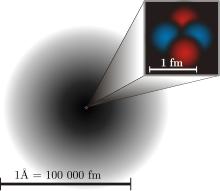
Questo mostra il modello atomico attuale. L'ombreggiatura nera intorno all'atomo mostra la probabilità di trovarvi un elettrone. Più è scura, più probabilità ci sono di trovare un elettrone in quel punto.
Pagine correlate
Cerca nell'enciclopedia