Termodinamica
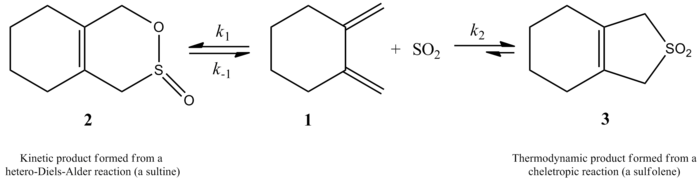
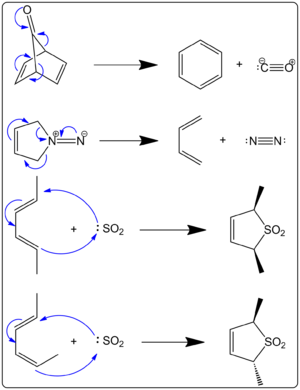
Quando l'anidride solforosa reagisce con butadiene e isoprene, si ottengono due prodotti diversi. Il meccanismo di reazione controllerà cosa viene prodotto. Un prodotto cinetico e un prodotto termodinamico sono entrambi possibili. Si ottiene più prodotto termodinamico che prodotto cinetico. Il prodotto cinetico viene da una reazione di Diels-Alder, mentre una reazione cheletropica fa un prodotto più termodinamicamente stabile. La via cheletropica è usata di più perché produce un addotto più stabile a cinque anelli. Lo schema qui sotto mostra la differenza tra i due prodotti. Il percorso a sinistra mostra il prodotto termodinamico, mentre il percorso a destra mostra il prodotto cinetico. Suarez e Sordo lo hanno dimostrato nel 1995. L'hanno dimostrato sia con gli esperimenti che usando i calcoli di Gaussian.
Cinetica
Un esempio di questo è la reazione cheletropica di 1,3-dieni con anidride solforosa. I chimici hanno esaminato attentamente la cinetica di questa reazione. Nel 1976, Isaacs e Laila hanno misurato i fattori cinetici per l'aggiunta di biossido di zolfo ai derivati del butadiene. I tassi di aggiunta sono stati monitorati in benzene a 30 °C con un eccesso iniziale di diene di venti volte. Hanno usato uno spettrofotometro per studiare la luce a 320 nm per misurare la scomparsa di SO2. La reazione ha mostrato una "pseudo cinetica di primo ordine". I chimici scoprirono che i gruppi che sottraggono elettroni al diene diminuivano il tasso di reazione. Inoltre, la velocità di reazione era influenzata considerevolmente dagli effetti sterici dei 2-sostituenti, con gruppi più ingombranti che aumentavano la velocità di reazione. (In altre parole, più grande è il gruppo di atomi che pende dal secondo atomo di carbonio, più veloce è la reazione). Gli autori attribuiscono questo alla tendenza dei gruppi ingombranti a favorire la conformazione cisoide del diene che è essenziale per la reazione (vedi tabella sotto). Inoltre, i tassi a quattro temperature sono stati misurati per sette dei dieni. Da queste misure, i chimici hanno usato l'equazione di Arrhenius per calcolare l'entalpia di attivazione (ΔH‡) e l'entropia di attivazione (ΔS‡) per ogni reazione. Questo è stato uno dei primi sforzi importanti per studiare la cinetica di una reazione cheletropica.
| -Butadiene | 104 k /min-1 (30 °C) (± 1-2%) assoluto | 104 k /min-1 (30 °C) (± 1-2%) relativo | ΔH‡ /kcal mol-1 | ΔS‡ /cal mol-1 K-1 |
| 2-metile | 1.83 | 1.00 | 14.9 | -15 |
| 2-etile | 4.76 | 2.60 | 10.6 | -20 |
| 2-isopropilico | 13.0 | 7.38 | 12.5 | -17 |
| 2-terz-butile | 38.2 | 20.8 | 10.0 | -19 |
| 2-neopentile | 17.2 | 9.4 | 11.6 | -18 |
| 2-cloro | 0.24 | 0.13 | N/A | N/A |
| 2-bromoetilico | 0.72 | 0.39 | N/A | N/A |
| 2-p-tolil | 24.7 | 13.5 | 10.4 | -19 |
| 2-fenile | 17.3 | 9.45 | N/A | N/A |
| 2-(p-bromofenile) | 9.07 | 4.96 | N/A | N/A |
| 2,3-dimetile | 3.54 | 1.93 | 12.3 | -18 |
| cis-1-metile | 0.18 | 0.10 | N/A | N/A |
| trans-1-metile | 0.69 | 0.38 | N/A | N/A |
| 1,2-dimetilene-cicloesano | 24.7 | 13.5 | 11.4 | -16 |
| 2-metil-1,1,4,4-d4 | 1.96 | N/A | N/A | N/A |
Monnat, Vogel e Sordo, nel 2002, hanno misurato la cinetica dell'aggiunta di biossido di zolfo a 1,2-dimetilidenecicloalcani. Hanno scritto che la reazione di 1,2-dimetilidenecicloesano con anidride solforosa può dare due prodotti diversi a seconda delle condizioni di reazione. La reazione produce la sultina corrispondente attraverso una reazione etero-Diels-Alder sotto controllo cinetico (≤ -60 °C), ma, sotto controllo termodinamico (≥ -40 °C), la reazione produce il sulfolene corrispondente attraverso una reazione cheletropica. L'entalpia di attivazione per la reazione etero-Diels-Alder è circa 2 kcal/mol più piccola di quella per la corrispondente reazione cheletropica. Il sulfolene è circa 10 kcal/mol più stabile della sultina isometrica in soluzione CH2Cl2/SO2.
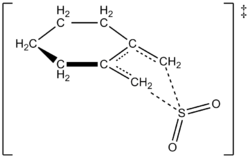
Gli autori sono stati in grado di elaborare sperimentalmente una legge di tasso a 261,2 K per la reazione di 1,2-dimetilidenecicloesano con anidride solforosa per dare il corrispondente sulfolene. La reazione era di primo ordine in 1,2-dimetilidenecicloesano ma di secondo ordine in anidride solforosa (vedi sotto). Questo ha confermato una previsione dei chimici teorici basata su calcoli quantistici ab initio di alto livello. Usando metodi computazionali, gli autori hanno proposto una struttura di transizione per la reazione cheletropica di 1,2-dimetilidenecicloesano con anidride solforosa (vedi figura a destra). La reazione è di secondo ordine nell'anidride solforosa perché un'altra molecola di anidride solforosa probabilmente si lega allo stato di transizione per contribuire a stabilizzarlo. Risultati simili sono stati trovati in uno studio del 1995 di Suarez, Sordo e Sordo che ha usato calcoli ab initio per studiare il controllo cinetico e termodinamico della reazione del biossido di zolfo con 1,3-dieni.
d [ 3 ] d t = k 2 [ 1 ] [ S O 2 ] 2 {displaystyle {frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}} ![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)
Effetti del solvente
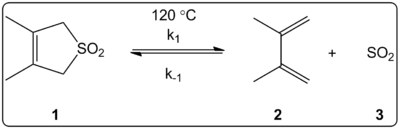
L'effetto del solvente della reazione cheletropica di 3,4-dimethyl-2,5-dihydrothiophen-1,1-dioxide (mostrato a destra) è stato studiato cineticamente in 14 solventi. Le costanti di velocità di reazione della reazione in avanti e inversa, oltre alle costanti di equilibrio, sono risultate essere linearmente correlate con la scala di polarità del solvente ET(30).
Le reazioni sono state fatte a 120 °C e sono state studiate con la spettroscopia 1H-NMR della miscela di reazione. La velocità in avanti k1 è risultata diminuire di un fattore di 4,5 passando dal cicloesano al metanolo. La velocità inversa k-1 è risultata aumentare di un fattore di 53 passando dal cicloesano al metanolo, mentre la costante di equilibrio Keq è diminuita di un fattore di 140. Si suggerisce che ci sia un cambiamento della polarità durante il processo di attivazione, come evidenziato dalle relazioni tra l'equilibrio e i dati cinetici. Gli autori dicono che la reazione sembra essere influenzata dalla polarità del solvente, e questo può essere dimostrato dal cambiamento dei momenti di dipolo quando si passa dal reagente allo stato di transizione al prodotto. Gli autori affermano anche che la reazione cheletropica non sembra essere influenzata né dall'acidità né dalla basicità del solvente.
I risultati di questo studio portano gli autori ad aspettarsi i seguenti comportamenti:
1. Il cambiamento della polarità del solvente influenzerà il tasso meno dell'equilibrio.
2. Le costanti di tasso saranno caratterizzate da un effetto opposto sulla polarità: k1 diminuirà leggermente con l'aumento di ET(30), e k-1 aumenterà nelle stesse condizioni.
3. L'effetto su k-1 sarà maggiore che su k1.

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)