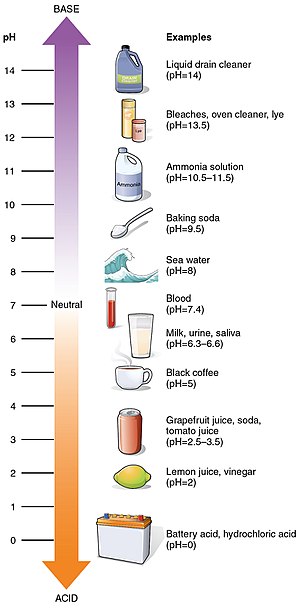
Il pH è una scala di acidità da 0 a 14. Dice quanto una sostanza sia acida o alcalina. Le soluzioni più acide hanno un pH più basso. Più soluzioni alcaline hanno un pH più alto. Le sostanze che non sono acide o alcaline (cioè le soluzioni neutre) hanno di solito un pH di 7. Gli acidi hanno un pH inferiore a 7. Gli alcali hanno un pH superiore a 7.
Il pH è una misura della concentrazione di protoni (H+) in una soluzione. S.P.L. Sørensen ha introdotto questo concetto nell'anno 1909. La p sta per il potenz tedesco, che significa potenza o concentrazione, e l'H per lo ione idrogeno (H+).
La formula più comune per il calcolo del pH è la seguente:
pH = - log 10 [ H + ] {\an8}- log _{\an8}mbox{pH}=-log _{10}left[mbox{H}H}^{+] right]} ![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
[H+] indica la concentrazione di ioni H+ (anche scritto [H3O+], l'uguale concentrazione di ioni idronio), misurata in moli per litro (conosciuta anche come molarità).
Tuttavia, l'equazione corretta è in realtà:
pH = - log 10 [ a H + ] {\an8}- log _{10} a sinistra[a_mathrm {H^{+] \an8} dx]. ![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)
dove uno stile di visualizzazione H + a_mathrm... }}  indica l'attività degli ioni H+. Ma, questa equazione nella maggior parte dei casi fornisce lo stesso valore della formula più comune, quindi in chimica introduttiva l'equazione precedente è data come definizione di pH.
indica l'attività degli ioni H+. Ma, questa equazione nella maggior parte dei casi fornisce lo stesso valore della formula più comune, quindi in chimica introduttiva l'equazione precedente è data come definizione di pH.
La maggior parte delle sostanze ha un pH compreso tra 0 e 14, anche se le sostanze estremamente acide o alcaline possono avere un pH < 0, o un pH > 14.
Le sostanze alcaline hanno, al posto degli ioni idrogeno, una concentrazione di ioni idrossido (OH-).
Domande e risposte
D: Che cos'è il pH?
R: Il pH è una scala di acidità da 0 a 14 che misura la concentrazione di protoni (H+) in una soluzione. Indica quanto è acida o alcalina una sostanza, con soluzioni più acide che hanno un pH più basso e soluzioni più alcaline che hanno un pH più alto. Le soluzioni neutre di solito hanno un pH pari a 7.
D: Chi ha introdotto il concetto di pH?
R: S.P.L. Sørensen ha introdotto questo concetto nel 1909.
D: Cosa significa la "p" in "pH"?
R: La "p" sta per la parola tedesca potenz, che significa potenza o concentrazione.
D: Come si calcola il pH?
R: La formula più comune per calcolare il pH consiste nel prendere il logaritmo negativo di 10 volte la concentrazione di ioni H+ (scritto anche [H3O+], che indica concentrazioni uguali di ioni idronio) misurata in moli per litro (o molarità). Tuttavia, esiste anche un'equazione che prende in considerazione l'attività invece della sola concentrazione, che può fornire valori diversi rispetto alla formula più comune, a seconda della situazione.
D: Che intervallo ha la maggior parte delle sostanze nella scala del pH?
R: La maggior parte delle sostanze ha un pH compreso tra 0 e 14, anche se le sostanze estremamente acide o alcaline possono avere un valore al di fuori di questo intervallo (inferiore a 0 o superiore a 14).
D: In che modo le sostanze alcaline sono diverse da quelle acide nella scala del pH? R: Le sostanze alcaline hanno valori più alti sulla scala a causa della loro concentrazione di ioni idrossido (OH-) anziché di ioni idrogeno come gli acidi.

![{\displaystyle {\mbox{pH}}=-\log _{10}\left[{\mbox{H}}^{+}\right]}](https://www.alegsaonline.com/image/093977a79b6a17e02db4699475930e48c05d6468.svg)
![{\displaystyle {\mbox{pH}}=-\log _{10}\left[a_{\mathrm {H^{+}} }\right]}](https://www.alegsaonline.com/image/7a631c4037415f3d4483a6cb07e69858b64890fc.svg)