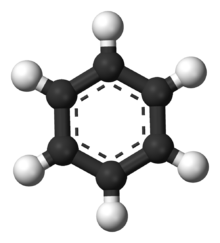
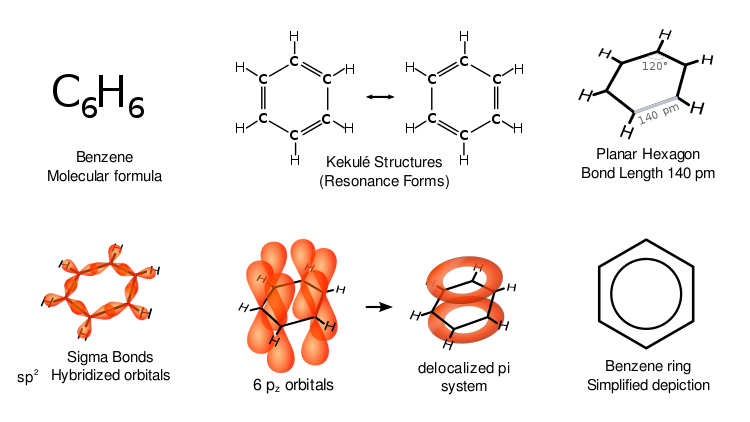Il benzene, talvolta chiamato benzolo, è un idrocarburo aromatico di formula C6H6 e nome comune benzolo. Si presenta come un liquido incolore a temperatura ambiente e altamente infiammabile, con un odore dolciastro caratteristico. La sua struttura fondamentale è un anello esagonale di sei atomi di carbonio, ciascuno legato a un idrogeno; la particolare distribuzione degli elettroni conferisce al sistema il comportamento tipico dei composti aromatici.
Struttura e proprietà chimiche
La stabilità del benzene deriva dalla delocalizzazione degli elettroni pi sull'anello, fenomeno spesso descritto mediante formule di risonanza. La molecola è planare e ogni atomo di carbonio è ibridato sp2. Chimicamente il benzene reagisce preferenzialmente per sostituzione elettrofila aromatica piuttosto che per addizione, perché così mantiene il sistema aromatico. In laboratorio e industria è utilizzato anche come solvente per molte sostanze organiche.
Produzione e fonti
Il benzene è presente in natura nel petrolio greggio e si ritrova come componente della benzina; per questo motivo viene emesso durante estrazione e raffinazione del petrolio (petrolio greggio) e durante la combustione. Industrialmente si ottiene da processi come il catalytic reforming o la distillazione frazionata e il cracking di idrocarburi, impiegati nelle raffinerie che forniscono anche combustibili come la benzina.
Usi ed esempi pratici
- Intermedio chimico per la produzione di materie plastiche e stirene (plastiche).
- Materia prima per gomma sintetica e additivi industriali (gomma sintetica).
- Sintesi di coloranti e prodotti chimici per tinture (coloranti).
- Uso come solvente in processi industriali e di laboratorio (solvente industriale).
- Presenza in alcuni prodotti farmaceutici come anello strutturale di composti più complessi (farmaci).
- Componente del carburante e additivo in miscele per motori (benzina).
Salute, ambiente e normative
Il benzene è riconosciuto come cancerogeno per l'uomo; l'esposizione prolungata o a livelli elevati aumenta il rischio di tumori del sangue e altre patologie ematologiche (può causare il cancro). Per questo esistono limiti di esposizione occupazionale e norme ambientali che regolano le emissioni. Essendo volatile e infiammabile, richiede precauzioni in stoccaggio e trasporto. La prevenzione include misure di contenimento, monitoraggio dell'aria e sostituzione con solventi meno pericolosi quando possibile.
Origine storica e curiosità
Il benzene è stato isolato nel XIX secolo dal catrame di carbone e il suo nome è legato al termine «benzoino», una resina usata in passato. La formulazione della struttura ad anello è attribuita a ricerche storiche che portarono al concetto moderno di aromaticità e alle prime rappresentazioni a sei lati. Oggi il benzene rimane una sostanza fondamentale nella chimica organica, oggetto sia di applicazioni industriali sia di controlli stringenti per la salute pubblica.
Per approfondire aspetti specifici come dati fisico‑chimici, normative o metodi di analisi, consultare risorse tecniche e documenti di sicurezza (benzolo, formula, proprietà fisiche, infiammabilità, aromaticità, valutazione del rischio, effetti sulla salute, benzina, materie plastiche, gomma sintetica, coloranti, solventi, petrolio greggio, farmaci contenenti anelli aromatici).

_1964,_MiNr_440.jpg)