Peptidi antimicrobici: definizione, meccanismi e potenziale terapeutico
Peptidi antimicrobici: scopri definizione, meccanismi d'azione e potenziale terapeutico come antibiotici ad ampio spettro e immunomodulatori contro batteri resistenti, virus e funghi.
I peptidi di difesa dell'ospite (o peptidi antimicrobici) fanno parte della risposta immunitaria innata e si riscontrano in tutte le classi di vita, dai batteri ai mammiferi. Sono piccole proteine o peptidi cationici e anfipatici che rappresentano una prima linea di difesa contro infezioni e danni tissutali.
Agiscono contro i microrganismi invasori. I peptidi uccidono i batteri Gram negativi e Gram positivi. Questo include i ceppi che sono resistenti agli antibiotici convenzionali. I peptidi agiscono anche contro i micobatteri (tra cui il Mycobacterium tuberculosis), i virus avvolti, i funghi e persino le cellule trasformate o cancerogene.
Questi peptidi sono eccellenti candidati per uso medico: integrano la terapia antibiotica convenzionale, presentano un'ampia gamma di attività e sono frequentemente battericidi (uccidono i batteri) piuttosto che batteriostatici (ne rallentano la crescita). Hanno bisogno di un tempo di contatto relativamente breve per esercitare la loro azione microbicida.
Ci sono grandi differenze tra le cellule procariotiche ed eucariotiche come bersaglio per i peptidi antimicrobici. Questi peptidi sono potenti antibiotici ad ampio spettro e, a differenza della maggior parte degli antibiotici tradizionali, molti di essi possiedono anche proprietà immunomodulatrici, cioè possono modulare la risposta infiammatoria e migliorare l'immunità dell'ospite.
Struttura e proprietà chimico-fisiche
I peptidi antimicrobici tipicamente sono corti (10–50 aminoacidi), ricchi di residui carichi positivamente (arginina, lisina) e possiedono regioni idrofobiche che consentono l'interazione con le membrane microbiche. La combinazione di carica positiva e carattere anfipatico favorisce l'attrazione verso le membrane negative dei microrganismi e la successiva destabilizzazione della membrana stessa. Esistono diverse famiglie note, tra cui le difensine, i catelicidine (es. LL-37), le magainine e le proteine batteriocine prodotte da batteri.
Meccanismi d'azione
I meccanismi non sono sempre unici e possono includere:
- Disgregazione della membrana: molti peptidi formano pori, destabilizzano la bicapa lipidica o inducono tensione di membrana, portando alla perdita di integrità e alla morte cellulare.
- Interferenza con bersagli intracellulari: alcuni penetrano la cellula e inibiscono sintesi di DNA, RNA o proteine, o legano componenti essenziali come il letale acido teicoico o gli enzimi metabolici.
- Modulazione della risposta infiammatoria: oltre all'azione microbicida, molti peptidi regolano la produzione di citochine, chemochine e l'attivazione di cellule immunitarie, contribuendo al controllo dell'infezione e alla riparazione dei tessuti.
- Attività antibiofilm: numerosi peptidi impediscono la formazione di biofilm o ne favoriscono la dispersione, migliorando l'efficacia degli antimicrobici e l'eliminazione delle infezioni croniche.
Spectrum d'attività e vantaggi
I peptidi antimicrobici mostrano attività verso batteri Gram-positivi e Gram-negativi, micobatteri, funghi e virus avvolti. Vantaggi principali:
- Rapidità d'azione
- Ampio spettro d'attività
- Bassa tendenza iniziale allo sviluppo di resistenza rispetto ad alcuni antibiotici tradizionali
- Proprietà immunomodulatorie che possono ridurre l'infiammazione e promuovere la guarigione
Limiti e sfide per l'uso terapeutico
Nonostante il potenziale, l'applicazione clinica presenta ostacoli:
- Tossicità per l'ospite: alcuni peptidi possono danneggiare cellule eucariotiche o essere emolitici a dosi elevate.
- Stabilità in vivo: degrado rapido da proteasi circolanti limita l'emivita; è spesso necessario modificare la sequenza per migliorarne la robustezza.
- Costi di produzione: la sintesi su larga scala e le modifiche chimiche possono essere costose.
- Consegna e formulazione: serve trovare veicoli che permettano il rilascio mirato e la riduzione della degradazione (liposomi, nanoparticelle, gel topici).
- Sviluppo di resistenza: benché più lento, non è impossibile che i patogeni sviluppino meccanismi di tolleranza o inattivazione.
Strategie per superare i limiti
Per aumentare il valore terapeutico si stanno studiando:
- Modifiche chimiche (D-amminoacidi, ciclizzazione, peptidomimetici) per aumentare stabilità e ridurre immunogenicità.
- Coniugazione a vettori o formulazioni avanzate (nanoparticelle, idrogel, rivestimenti per dispositivi medici).
- Combinazioni con antibiotici convenzionali per sfruttare sinergie e prevenire resistenze.
- Design razionale e screening ad alto rendimento per identificare sequenze ottimali con bassa tossicità e alta efficacia.
Esempi e stato clinico
Alcuni peptidi sono già approvati o in fase avanzata di sperimentazione clinica per infezioni cutanee, ulcere, e come rivestimenti per dispositivi. Peptidi noti in letteratura includono le difensine e la catelicidina umana LL-37, magainine (provenienti da rana) e numerosi peptidi sintetici ottimizzati per uso clinico. La ricerca continua a valutare indicazioni diverse, dalla terapia delle ferite infette alla lotta contro batteri multiresistenti e biofilm associati a protesi.
Prospettive future
La combinazione di biologia sintetica, chimica dei peptidi e nanotecnologie promette di accelerare lo sviluppo di peptidi antimicrobici terapeutici. L'approccio ideale probabilmente sarà multimodale: peptidi ottimizzati per stabilità e sicurezza, veicolati con sistemi di rilascio mirati e impiegati in combinazione con trattamenti convenzionali per ridurre l'emergere di resistenza e migliorare gli esiti clinici.
Conclusione: i peptidi antimicrobici rappresentano una promettente classe di agenti terapeutici che uniscono attività microbicida diretta e modulazione immunitaria. Superare le sfide di stabilità, tossicità e costo è essenziale per tradurre il loro potenziale in trattamenti sicuri ed efficaci.
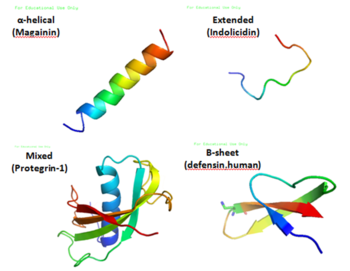
Varie strutture di peptidi antimicrobici
Pagine correlate
Domande e risposte
D: Che cos'è un peptide di difesa dell'ospite o un peptide antimicrobico?
R: Un peptide di difesa dell'ospite (o peptide antimicrobico) è una parte della risposta immunitaria innata che agisce contro i microrganismi invasori.
D: Quali tipi di organismi sono colpiti dai peptidi di difesa dell'ospite?
R: I peptidi di difesa dell'ospite uccidono i batteri Gram negativi e Gram positivi, i micobatteri (compreso il Mycobacterium tuberculosis), i virus avvolti, i funghi e persino le cellule trasformate o cancerose.
D: I peptidi di difesa dell'ospite funzionano contro i batteri resistenti agli antibiotici?
R: Sì, i peptidi di difesa dell'ospite funzionano contro i ceppi di batteri resistenti agli antibiotici convenzionali.
D: I peptidi di difesa dell'ospite sono adatti all'uso medico?
R: Sì, i peptidi di difesa dell'ospite sono ottimi candidati per l'uso medico, perché integrano la terapia antibiotica convenzionale e hanno un'ampia gamma di attività.
D: In che modo i peptidi di difesa dell'ospite differiscono dagli antibiotici convenzionali?
R: I peptidi di difesa dell'ospite sono battericidi anziché batteriostatici, ossia uccidono i batteri anziché limitarsi a inibirne la crescita. Inoltre, richiedono solo un breve tempo di contatto per uccidere i batteri.
D: I peptidi di difesa dell'ospite agiscono sulle cellule eucariotiche?
R: I peptidi di difesa dell'ospite presentano grandi differenze tra le cellule procariotiche ed eucariotiche come bersaglio. Non sono dannosi per le cellule eucariotiche, ma solo per i microrganismi invasori.
D: I peptidi di difesa dell'ospite possono migliorare l'immunità?
R: Sì, la ricerca suggerisce che i peptidi di difesa dell'ospite possono migliorare l'immunità lavorando come immunomodulatori, che rafforzano il sistema immunitario.
Cerca nell'enciclopedia