Amminoacido
Gli amminoacidi sono gli elementi costitutivi delle proteine. Negli eucarioti, ci sono 20 amminoacidi standard di cui sono fatte quasi tutte le proteine.
In biochimica, un amminoacido è una qualsiasi molecola che ha sia gruppi funzionali amminici (NH2+R) che carbossilici (C=O). In biochimica, questo termine si riferisce agli alfa-amminoacidi con la formula generale H2NCHRCOOH, dove R è uno dei molti gruppi laterali (vedi diagramma).
Sono noti circa 500 amminoacidi. Per gli animali, la cosa più importante che gli aminoacidi fanno è produrre proteine, che sono catene di aminoacidi molto lunghe. Ogni proteina ha la sua propria sequenza di amminoacidi, e questa sequenza fa sì che la proteina assuma forme diverse e abbia funzioni diverse. Gli amminoacidi sono come l'alfabeto delle proteine; anche se si hanno solo poche lettere, se le si collega, si possono fare molte frasi diverse.
Nove dei 20 amminoacidi standard sono amminoacidi "essenziali" per l'uomo. Non possono essere costruiti (sintetizzati) da altri composti dal corpo umano, e quindi devono essere assunti come cibo. Altri possono essere essenziali per alcune età o condizioni mediche. Gli amminoacidi essenziali possono anche differire da una specie all'altra. Gli erbivori devono ottenere i loro aminoacidi essenziali dalla loro dieta, che per alcuni è quasi interamente erba. I ruminanti come le mucche ottengono alcuni aminoacidi attraverso i microbi nelle prime due camere dello stomaco.
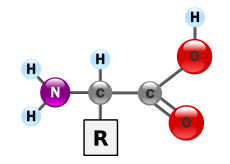
Gli amminoacidi sono il prodotto finale delle proteine. La struttura generale di un α-amminoacido, con il gruppo amminico a sinistra e il gruppo carbossilico a destra.
Struttura
Un amminoacido è un prodotto chimico organico. È costituito da un atomo di α-carbonio che è legato covalentemente a quattro gruppi.
- un atomo di idrogeno
- un gruppo amino (-NH2)
- un gruppo carbossile (-COOH)
- un gruppo R variabile
Ogni amminoacido ha almeno un gruppo amminico (-NH2) e un gruppo carbossilico (-COOH), eccetto la prolina.
Espressione genica e biochimica
Questi sono gli aminoacidi proteogenici, che sono i mattoni per le proteine. Sono prodotti da macchinari cellulari codificati nel codice genetico di qualsiasi organismo.
| Aminoacido | Breve | Abbrev. | Codon(i) | Occorrenzein | Essenziale‡ negli esseri umani |
| A | Ala | GCU, GCC, GCA, GCG | 7.8 | No | |
| C | Cys | UGU, UGC | 1.9 | A condizione che | |
| Acido aspartico | D | Asp | GAU, GAC | 5.3 | No |
| Acido glutammico | E | Glu | GAA, GAG | 6.3 | A condizione che |
| Fenilalanina | F | Phe | UUU, UUC | 3.9 | Sì |
| Glycine | G | Gly | GGU, GGC, GGC, GGA, GGG | 7.2 | A condizione che |
| Istidina | H | Il suo | CAU, CAC | 2.3 | Sì |
| Isoleucina | I | Ile | AUU, AUC, AUA | 5.3 | Sì |
| Lisina | K | Lys | AAA, AAG | 5.9 | Sì |
| Leucine | L | Leu | UUA, UUG, CUU, CUC, CUC, CUA, CUG | 9.1 | Sì |
| Metionina | M | Incontrato | AUG | 2.3 | Sì |
| Asparagina | N | Asn | AAU, AAC | 4.3 | No |
| Pirrolisina | O | Pyl | UAG* | 0 | No |
| Proline | P | Pro | CCU, CCC, CCA, CCG | 5.2 | No |
| Glutammina | Q | Gln | CAA, CAG | 4.2 | No |
| Arginina | R | Arg | CGU, CGC, CGA, CGG, AGA, AGG | 5.1 | A condizione che |
| Serine | S | Ser | UCU, UCC, UCA, UCG, AGU, AGU, AGC | 6.8 | No |
| Treonina | T | Thr | ACU, ACC, ACA, ACA, ACG | 5.9 | Sì |
| Selenocisteina | U | Sec | UGA** | >0 | No |
| Valine | V | Val | GUU, GUC, GUA, GUA, GUG | 6.6 | Sì |
| W | Trp | UGG | 1.4 | Sì | |
| Y | Tyr | UAU, UAC | 3.2 | A condizione che | |
| Codone di arresto† | - | Termine | UAA, UAG, UGA††† | - | - |
* UAG è normalmente il codice di stop ambra, ma codifica la pirrolisina se è presente un elemento PYLIS.
** UGA è normalmente il codone di stop opale (o umber), ma codifica la selenocisteina se è presente un elemento SECIS.
† Il codone di stop non è un amminoacido, ma è incluso per completezza.
†† UAG e UGA non sempre agiscono come codici di stop (vedi sopra).
‡ Un amminoacido essenziale non può essere sintetizzato nell'uomo. Deve essere fornito nella dieta. Gli amminoacidi essenziali non sono normalmente richiesti nella dieta, ma devono essere forniti alle popolazioni che non ne fanno abbastanza.
A questi α-amminoacidi ulteriormente nei processi di biosintesi che appaiono non essenziali sono strutturalmente (qui utilizzando la notazione SMILES) relativi:
OC(=O)C(N)-
- ├ H ... V Glycine
- ├ C ... P Alanine
- │├ C ... acido 2-aminobutirrico
- ││├ C ... Norvaline
- ││││├ -2H ... _ Proline (deidronorvalina)
- ││││├ C ... Norleucina
- │││││└ N ... Z Lisina
- │││││ └ C(=O)C1N=CCC1C ... ^ Pirrolisina
- ││││└ NC(=N)N ... a Arginina
- ││├ C(=O)N ... ` Glutammina
- ││├ C(=O)O ... T Acido glutammico
- ││├ O ... Omoserina
- ││└ S . ... Omocisteina
- ││ └ C ... \ Metionina
- │├ C(C)C ... [ Leucine
- │├ C(=O)N ... ] Asparagine
- │├ C(=O)O ... S Acido aspartico
- │├ C1=CNC=N1 ... W Istidina
- │├ c1ccccccc1 ... U Fenilalanina
- │├ c1ccc(O)cc1 ... h Tirosina
- │├ C1=CNc2ccccccc12 ... f Triptofano
- │├ C1=CNc2cccc(O)cc12 ... Oxitriptan
- │├ c(cc1I)cc(I)cc(I)c1-O-c2cc(I)c(O)c(I)c2 ... Tiroxina
- │├ O ... b Serine
- │├ S ... R Cisteina
- │└ [SeH] ... d Selenocisteina
- ├ C(C)C ... e Valine
- ├ C(C)O ... c Treonina
- └ C(C)CC ... X Isoleucine
Domande e risposte
D: Cosa sono gli aminoacidi?
R: Gli aminoacidi sono molecole che hanno sia gruppi funzionali amminici (NH2+R) che carbossilici (C=O) e sono i mattoni delle proteine.
D: Quanti aminoacidi "standard" esistono negli eucarioti?
R: Negli eucarioti, ci sono 20 aminoacidi "standard" di cui sono composte quasi tutte le proteine.
D: Qual è la formula generale degli alfa-amminoacidi?
R: La formula generale degli alfa-amminoacidi è H2NCHRCOOH, dove R è uno dei tanti gruppi laterali.
D: A cosa si riferisce la biochimica quando parla di aminoacidi?
R: In biochimica, il termine 'aminoacido' si riferisce agli alfa-amminoacidi con la formula generale H2NCHRCOOH, dove R è uno dei tanti gruppi laterali.
D: Come si strutturano le proteine?
R: Le proteine ottengono la loro struttura dalla combinazione di diversi tipi di aminoacidi.
D: Che ruolo hanno i gruppi funzionali amminici e carbossilici in una molecola di aminoacido?
R: I gruppi funzionali amminico e carbossilico costituiscono una molecola di amminoacido; forniscono un atomo di azoto e un atomo di carbonio che possono formare legami con altre molecole.
Cerca nell'enciclopedia