Nella chimica organica, una reazione elettrociclica è un tipo di reazione di riordinamento periciclico. La reazione è elettrociclica se il risultato è un legame pi greco che diventa un legame sigma o un legame sigma che diventa un legame pi greco. Le reazioni elettrocicliche hanno le seguenti proprietà:
- le reazioni elettrocicliche sono guidate dalla luce (fotoindotta) o dal calore (termica)
- il modo di reazione è determinato dal numero di elettroni pi nella parte con più legami pi
- una reazione elettrociclica può chiudere un anello (elettrocilizzazione) o aprire un anello
- la stereospecificità è determinata da una formazione di stato di transizione conrotatoria o disrotatoria, come previsto dalle regole di Woodward-Hoffmann.
La torquoselettività in una reazione elettrociclica si riferisce alla direzione di rotazione dei sostituti. Ad esempio, i sostituenti in una reazione che è conrotatoria possono ancora ruotare in due direzioni. Essa produce una miscela di due prodotti che sono l'immagine speculare l'uno dell'altro (prodotti enantiomerici). Una reazione che è torquoselettiva limita uno di questi sensi di rotazione (parzialmente o completamente) per produrre un prodotto in eccesso enantiomerico (dove uno stereoisomero è prodotto molto più dell'altro).
I chimici sono interessati alle reazioni elettrocicliche perché la geometria delle molecole conferma una serie di previsioni fatte dai chimici teorici. Esse confermano la conservazione della simmetria molecolare orbitale.
La reazione di ciclizzazione di Nazarov è una reazione elettrociclica che chiude un anello. Converte i divinilchetoni in ciclopentenoni. (Fu scoperta da Ivan Nikolaevich Nazarov (1906-1957).
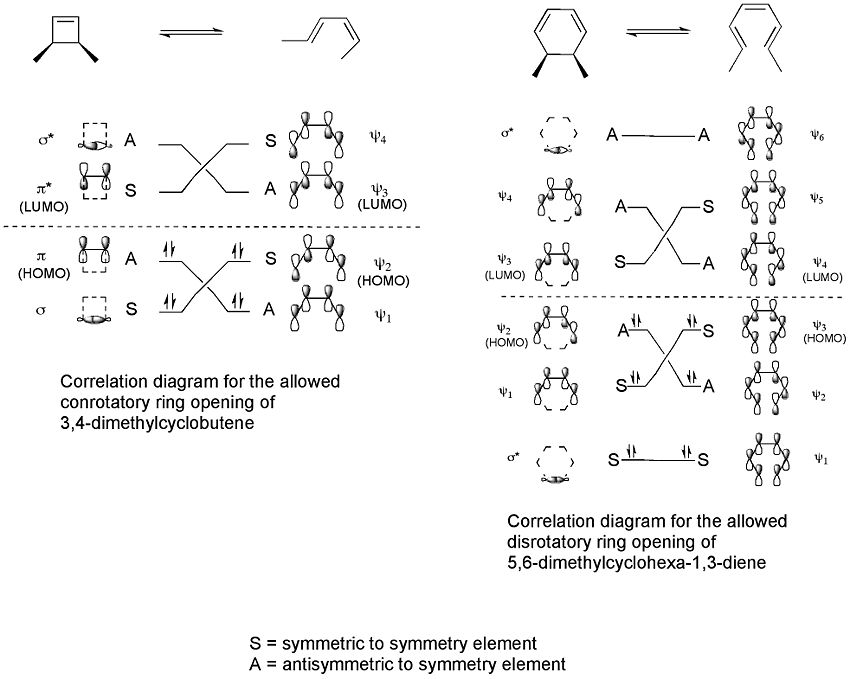
Un esempio è la reazione termica di apertura ad anello del 3,4-dimetilciclobutene. L'isomero cis produce solo cis,trans-2,4-esadiene. Ma l'isomero trans dà il trans,trans diene:
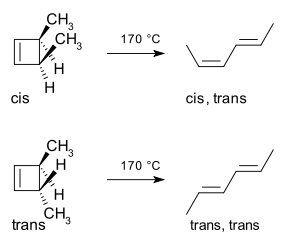
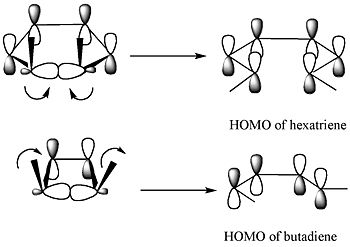
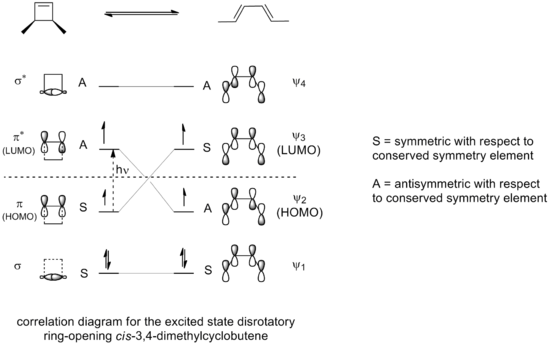
Il metodo della frontiera orbitale spiega come funziona questa reazione. Il legame sigma nel reagente si aprirà in modo che i p-orbitali risultanti avranno la stessa simmetria dell'orbitale molecolare più alto occupato (HOMO) del prodotto (un butadiene). Questo può accadere solo con un'apertura ad anello conrotatorio che si traduce in segni opposti per i due lobi alle estremità rotte dell'anello. (Un'apertura ad anello disrotatorio formerebbe un anti-bond.) Il seguente diagramma lo mostra:
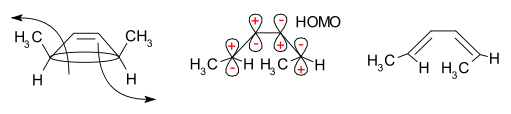
La stereospecificità del risultato dipende dal fatto che la reazione proceda attraverso un processo conrotatorio o disrotatorio.