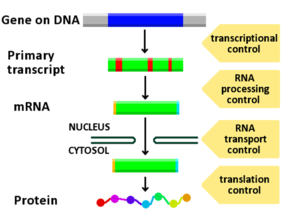
L'espressione genica è il processo attraverso il quale l'informazione ereditabile in un gene, la sequenza di coppie di basi del DNA, viene trasformata in un prodotto genico funzionale, come una proteina o un RNA. L'idea di base è che il DNA viene trascritto in RNA, che viene poi tradotto in proteine. Le proteine costituiscono molte delle strutture cellulari e spiegano l'attività di gran parte degli enzimi presenti in una cellula o in un intero organismo.
Diverse fasi del processo di espressione genica possono essere modulate (sintonizzate). Questo include sia la trascrizione che la traduzione, oltre agli eventi successivi come il ripiegamento e le modifiche post-traduzionali di una proteina. La regolazione genica accende e spegne i geni, e quindi controlla la differenziazione cellulare e la morfogenesi. La regolazione genica può anche servire come base per il cambiamento evolutivo: il controllo dei tempi, della posizione e della quantità dell'espressione genica può avere un effetto profondo sullo sviluppo e sull'adattamento degli organismi.
Un singolo gene può avere livelli di espressione diversi in tessuti differenti e produrre effetti multipli a seconda del contesto cellulare: questo fenomeno è legato al concetto di pleiotropismo, un tema centrale in genetica.
Meccanismi fondamentali
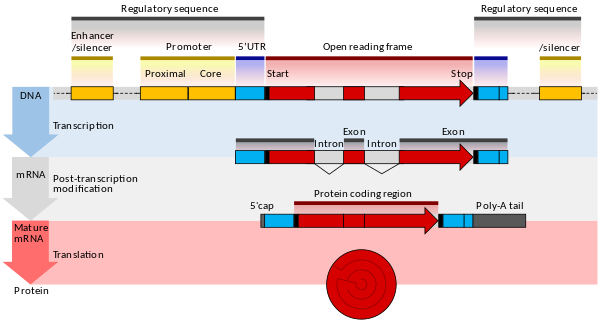
- Trascrizione: l'RNA polimerasi si lega al promotore del gene e sintetizza una molecola di RNA complementare al filamento di DNA. Fattori di trascrizione e elementi regolatori (promotori, enhancer, silencer) modulano l'avvio e l'intensità della trascrizione.
- Processing dell'RNA: negli eucarioti l'RNA primario subisce capping 5', poliadenilazione 3' e splicing (rimozione degli introni). Questi passaggi determinano la stabilità, l'esportazione nucleare e l'efficienza di traduzione dell'mRNA.
- Traduzione: i ribosomi leggono la sequenza dell'mRNA in codoni e assemblano gli amminoacidi nella proteina corrispondente. Fattori di inizio, elongazione e terminazione controllano la velocità e l'accuratezza del processo.
- Modifiche post-traduzionali e ripiegamento: dopo la sintesi, le proteine possono essere fosforilate, glicosilate, ubiquitinate, e subire altri interventi chimici; chaperoni molecolari aiutano il corretto ripiegamento e il traffico intracellulare.
- Degradazione: la regolazione del livello proteico dipende anche dalla degradazione selettiva (es. sistema ubiquitina-proteasoma, autofagia).
Regolazione dell'espressione genica
La regolazione avviene a molti livelli e utilizza meccanismi diversificati:
- Regolazione trascrizionale: fattori di trascrizione, coattivatori e corepressori modulano l'accessibilità del promotore; enhancers e insulator influenzano l'attività a distanza.
- Controlli epigenetici: la metilazione del DNA e le modifiche degli istoni (acetilazione, metilazione, fosforilazione) alterano la struttura della cromatina e quindi la probabilità che un gene venga trascritto.
- RNA non codificanti: microRNA (miRNA), small interfering RNA (siRNA) e long non-coding RNA (lncRNA) regolano la stabilità e la traduzione degli mRNA o modulano direttamente l'espressione trascrizionale.
- Regolazione post-trascrizionale: controllo dello splicing alternativo, editing dell'RNA, localizzazione subcellulare e degradazione mediata da vie specifiche.
- Controllo translazionale: meccanismi che influenzano l'inizio della traduzione (es. 5'UTR strutturale, upstream open reading frames) e la disponibilità dei fattori di traduzione.
Ruolo nello sviluppo e nell'evoluzione
Il profilo di espressione genica varia nel tempo e nello spazio durante lo sviluppo: la stessa sequenza genica può produrre risposte diverse a seconda del tessuto, dello stadio di sviluppo e degli stimoli ambientali. Modifiche nei circuiti di regolazione (più che cambiamenti nelle proteine stesse) sono spesso alla base di differenze fenotipiche tra specie e di innovazioni evolutive.
Tecniche per studiare l'espressione genica
- RT-qPCR e Northern blot per la quantificazione di RNA specifici.
- RNA-seq e microarray per profili globali di trascrittoma; single-cell RNA-seq per analisi a cellula singola.
- Western blot e spettrometria di massa per l'analisi delle proteine.
- ChIP-seq per identificare siti di legame di fattori di trascrizione e marcature istoniche.
- Saggi di reporter (es. GFP), ibridazione in situ e imaging per visualizzare l'espressione spaziale.
Implicazioni cliniche e applicazioni
Alterazioni nell'espressione genica sono alla base di molte malattie: mutazioni nei promotori o negli enhancer, difetti epigenetici, espressione aberrante di microRNA e disfunzioni nei meccanismi di degradazione possono portare a cancro, malattie neurodegenerative, disordini metabolici e altre patologie. La modulazione dell'espressione genica è alla base di approcci terapeutici moderni, come:
- terapie geniche e di editing (CRISPR/Cas) per correggere o modulare l'espressione genica;
- uso di RNA interference e oligonucleotidi antisenso per ridurre l'espressione di geni patologici;
- farmaci epigenetici che modificano metilazione del DNA o modifiche istoniche.
In sintesi, l'espressione genica è un processo dinamico e multilivello che determina come l'informazione contenuta nel DNA si traduca in funzione biologica. Comprendere i suoi meccanismi è fondamentale per la biologia dello sviluppo, la medicina e le biotecnologie.