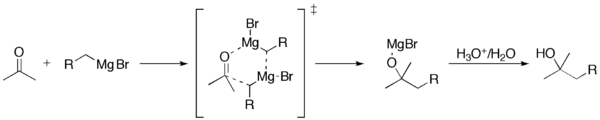
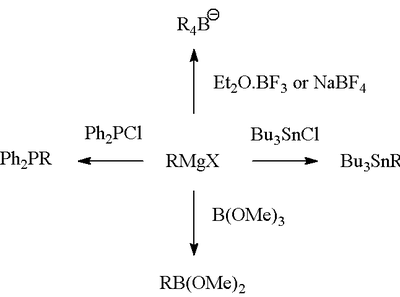
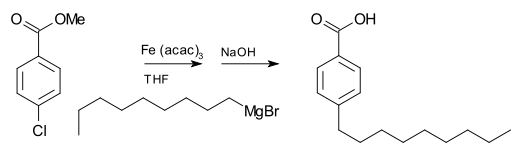
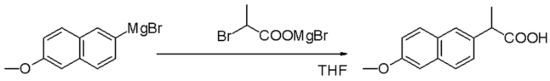
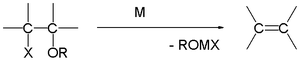
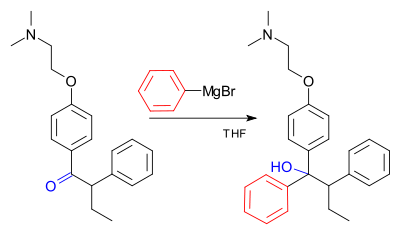
La reazione di Grignard (pronunciato /ɡriɲar/) è una reazione chimica organometallica in cui gli alogenuri alchilici o arilmagnesici (reagenti di Grignard) attaccano gli atomi di carbonio elettrofilici presenti all'interno dei legami polari (ad esempio, in un gruppo carbonilico come nell'esempio riportato di seguito). I reagenti di Grignard agiscono come nucleofili. La reazione di Grignard produce un legame carbonio-carbonio. Essa altera l'ibridazione del centro di reazione. La reazione di Grignard è uno strumento importante nella formazione dei legami carbonio-carbonio. Può anche formare legami carbonio-fosforo, carbonio-stagno, carbonio-silicio, carbonio-boro e altri legami carbonio-eteroatomici.
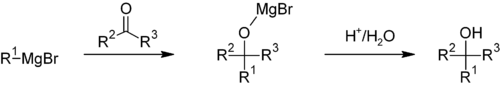
Si tratta di una reazione di addizione organometallica nucleofila. L'alto valore pKa della componente alchilica (pKa = ~45) rende la reazione irreversibile. Le reazioni di Grignard non sono ioniche. Il reagente di Grignard esiste come cluster organometallico (in etere).
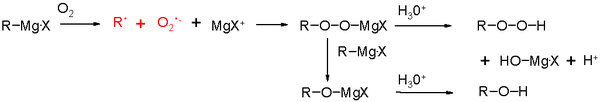
Lo svantaggio dei reagenti di Grignard è che reagiscono prontamente con solventi protici (come l'acqua), o con gruppi funzionali con protoni acidi, come alcoli e ammine. L'umidità atmosferica può alterare la resa di fabbricazione di un reagente di Grignard da torniture di magnesio e da un alogenuro alchilico. Uno dei molti metodi utilizzati per escludere l'acqua dall'atmosfera di reazione è quello di essiccare a fiamma il recipiente di reazione per far evaporare tutta l'umidità, che viene poi sigillato per evitare che l'umidità ritorni. I chimici utilizzano poi gli ultrasuoni per attivare la superficie del magnesio in modo che consumi l'acqua presente. Questo può permettere ai reagenti di Grignard di formarsi con una minore sensibilità all'acqua presente.
Un altro svantaggio dei reagenti di Grignard è che non formano facilmente legami carbonio-carbonio reagendo con gli alogenuri alchilici con un meccanismoSN2.
François Auguste Victor Grignard ha scoperto le reazioni e i reagenti di Grignard. Prendono il nome da questo chimico francese (Università di Nancy, Francia) che per questo lavoro ha ricevuto il premio Nobel per la chimica del 1912.